Hidrojen Bağının Kaynama Noktasına Etkisi • Hidrojen bağı zayıf etkileşimler arasında en kuvvetli olanıdır. Bir yapıda hidrojen
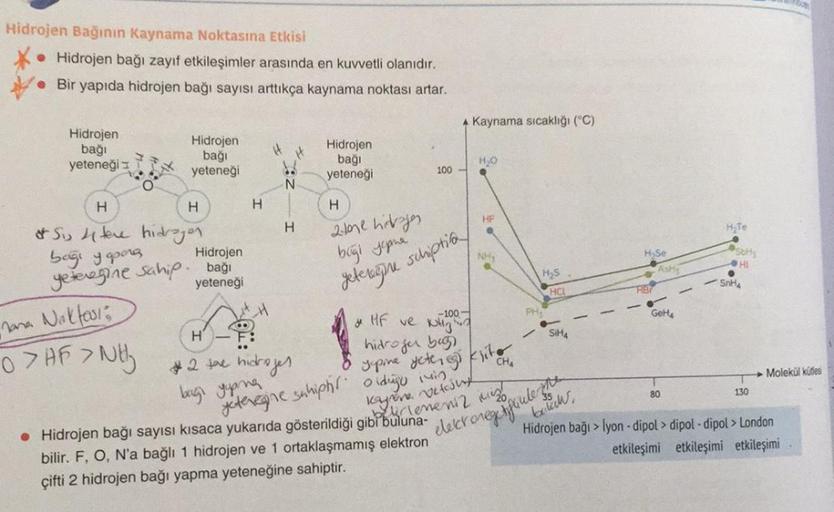
Hidrojen Bağının Kaynama Noktasına Etkisi • Hidrojen bağı zayıf etkileşimler arasında en kuvvetli olanıdır. Bir yapıda hidrojen bağı sayısı arttıkça kaynama noktası artar. Hidrojen bağı yeteneği Hidrojen bağı yeteneği H H Si te hidrogen bağı y apora Hidrojen yeteneğine sahip. bağı yeteneği Mana Nakfasi 07AF, NJ H & H H H H 6. N H H 2 the hidroges bagi yupna Hidrojen bağı yeteneği H 2-tone hajen baği yapma yeteneğine 100 schiptio A Kaynama sıcaklığı (°C) -100- yeteneğine sahiphs oldugu ivin, kayure bel • Hidrojen bağı sayısı kısaca yukarıda gösterildiği gibi buluna- bilir. F, O, N'a bağlı 1 hidrojen ve 1 ortaklaşmamış elektron çifti 2 hidrojen bağı yapma yeteneğine sahiptir. H₂O ● HF NH₂ & HF ve K hidrogen beg yupine yote ikite CH4 H₂S one vetojux leneniz iz PH. HCL SIHA H₂Se HB ASHE GeH 80 H₂Te Sols HI ● SnH₂ 130 balaw, elecronegeifuule the Hidrojen bağı > lyon -dipol > dipol-dipol > London etkileşimi etkileşimi etkileşimi Molekül kütles
