Kimya Soruları
TYT, AYT, YKS, LGS, KPSS, ALES hazırlık sürecinde dilediğin dersten soru çözüm desteği almak ister misin? Kunduz’a sorularını sor, alanında uzman eğitmenler cevaplasın.

Kimya
Zayıf Etkileşimler7. I. He(s)
II. C₂H(S)
III. CHCl (s)
heimfaollata
Yukarıdaki sıvıların aynı ortamda kaynamaya başlama
sıcaklıkları arasındaki ilişki nasıldır? (H, He.6C.17Cl)
10.1. HBr(s)
11. CCI (S
III. NHS
Yukarıd
leri ara

Kimya
Bağ Enerjileri ve Hess Yasasıar
Boş: Net:.
RLİĞİ
X+ 2Y
Y+T
Z
M
cifci
sidir?
SINAV
Büyük Düşün Hedefini Yüksek Tut
AH₁ = a
AH₂ = b
AH₂ = C
X+T-K
olduğuna göre,
Z+3TK + 2M AH₁
tepkimesinin
nedir?
A) a + b + c
esinin entalp
entalpi değişim değeri (AH₂)
B) 2b + a + c
TEST 31
D) 2b + c - a
O
Cla) +
C) 2b-(a+c)
E) 2a - (b + c)
D(g) + 50

Kimya
Karışımları Ayırma Teknikleri19. Bir grup öğrenci, öğretmenlerinin verdiği performans öde-
vini yapmak için aşağıdaki deney düzeneğini hazırlamıştır.
Deneme - 2
Hazırladıkları bu deney düzeneğinde bir bağırsak parça-
sının içine glikoz ve nişasta çözeltisi koyarak bu bağır-
sak çözeltisini bir ip ile tutturup şekildeki gibi sabitliyorlar.
Daha sonra bağırsak parçasını, içerisinde saf su bulu-
nan bir deney kabına koyuyorlar.
lyot
Saf su
Glikoz + nişasta
çözeltisi
Bir süre bekledikten sonra içerisinde saf su bulunan
deney kabına iyot damlatarak deney süresince mey-
dana gelen olayları not ediyorlar. Sonra bu notlarını şu
şekilde düzenliyorlar:
Kaptaki saf su miktarında azalma meydana gelmiştir.
II Kaptaki iyot mavi-mor renge boyanır.
III. Kap ve bağırsak parçasındaki glikoz miktarı eşitlenir.
A) Yalnız I
Buna göre, öğrenci grubu not ettiği olaylardan
hangisinde yanlışlık yapmamıştır?
(Nişasta iyot varlığında mavi-mor renk alır.)
D) Il ve Ill
B) I ve II
E) I, II ve III
C) I ve III
20 Kan gruplarının tayininde Hasan'ın kan plazmasında sa-
![e 3
n-
a-
le
n-
5.
103
7₂0]
b.
CO
a
Sh
Derişim (mol/L)
Y
ne ilişkin;
HORSE
x k
O
62 311
Zaman
2X(g) 3Y(g)
C
tepkimesi için maddelerin molar deri-
le pob hekonstne
şimlerinin zamanla değişimi grafikteki
gibidir.
3
never I'den
Belli bir sıcaklıktaki denge sistemini
lomuloet DiabığSSA
1. Derişim türünden denge sabiti dir.
Denge sabiti 1 den büyüktür.
Il Başlangıçta kapta sadece X bulunur.
(1
t anında dengeye ulaşmıştır.
Palme Yayınevi
bijck.
yargılarından hangileri doğrudur?
A) Yalnız II
B) II ve III
678
C) I ve III
SYA
D) II, III ve IV E) I, III ve IV
Bi tepk
tüm tep
Denge sabihi
tepkime
ya da ür
durumda
celiğin he
kimenin g
1616
tırılması g
dir. İle
63
Zinda
Okayar
gelir.
Qc
dir. G
hızınc
90433
kayar
gelir.
> Q'c =
eşittin
tepkin
maz.](https://media.kunduz.com/media/question/seo/raw/20230323160031449020-2479465.jpeg?w=256)
Kimya
Kimyanın Temel Kanunlarıe 3
n-
a-
le
n-
5.
103
7₂0]
b.
CO
a
Sh
Derişim (mol/L)
Y
ne ilişkin;
HORSE
x k
O
62 311
Zaman
2X(g) 3Y(g)
C
tepkimesi için maddelerin molar deri-
le pob hekonstne
şimlerinin zamanla değişimi grafikteki
gibidir.
3
never I'den
Belli bir sıcaklıktaki denge sistemini
lomuloet DiabığSSA
1. Derişim türünden denge sabiti dir.
Denge sabiti 1 den büyüktür.
Il Başlangıçta kapta sadece X bulunur.
(1
t anında dengeye ulaşmıştır.
Palme Yayınevi
bijck.
yargılarından hangileri doğrudur?
A) Yalnız II
B) II ve III
678
C) I ve III
SYA
D) II, III ve IV E) I, III ve IV
Bi tepk
tüm tep
Denge sabihi
tepkime
ya da ür
durumda
celiğin he
kimenin g
1616
tırılması g
dir. İle
63
Zinda
Okayar
gelir.
Qc
dir. G
hızınc
90433
kayar
gelir.
> Q'c =
eşittin
tepkin
maz.

Kimya
Karışımların Genel Özellikleri12. Birbiri içinde dağılan maddeler, dağılma büyüklüklerine
göre homojen veya heterojen karışım oluştururlar.
Dağılan taneceklerin boyutu 1000 nm'den büyük bir
karışımı süspansiyon olarak adlandıran bir öğrenci,
aşağıdaki açıklamalardan hangisini yaparsa yanlış
olur?
A) Karışım, çamurlu su olabilir.
B) Kanşım, katının sivi içinde çözünmesi ile gerçekle-
şir..
of Karışım, heterojendir.
Dy Dağılan parçacıklar gözle görülebilir.
E) Karışım biraz bekletilirse çökme olur.

Kimya
Çözücü Çözünen Etkileşimleri6. Kütlece %40 lık 400 gr tuzlu su çözeltisi yine aynı sıcaklıkta kütlece %10 luk 200
gram tuzlu su çözeltisi karıştırılırsa son durumda kütlece yüzde derişimi ne olur?
7. Koligatif özellik nedir ?
8. Donma noktası alçalmasını tanımlayınız 3 örnek veriniz.
9. Kaynama noktası yükselmesini tanımlayınız. Örnek veriniz.
10. Suyun içine aşağıdaki maddeler eklenerek karıştırılıyor. Hangilerinde çözünme
olur hangilerinde olmaz nedeniyle açıklayınız.
a) CC14
b) NH3
c) CH3OH
(Su polar, CC14 apolar, NH3 polar, CH3OH polardır.)

Kimya
Asitler ve Bazlar441
Pkaj
11. HX ve HY asitlerinden pka değeri daha büyük olanı HX'tir.
Aynı sıcaklıktaki eşit derişimli HX ve HY sulu çözeltileri ile
ilgili,
I. HX daha kuvvetli asittir.
II. pH'ları arasında HY > HX ilişkisi vardır.
III. Asitlik sabitleri arasında (Ka) HY > HX ilişkisi vardır.
yargılarından hangileri yanlıştır?
A) Yalnız I
B) Yalnız II
Na
D) I ve III
6-10
Jou
E) I, II ve III
C) I ve II

Kimya
Tepkimelerde Isı Değişimi15. 3,9 g X in aşırı miktarda su ile tepkimesinden XOH ve
H₂ oluşurken 20 kJ ısı açığa çıkıyor.
XH nin oluşma entalpisi - 60 kJ/mol olduğuna göre,
XH + H₂O → XOH + H₂
tepkimesinin AH değeri kaçtır?
(X: 39)
A) - 260
60-80
D) - 140
B) - 240
E) +140
AH = -20
C) +240

Kimya
Kimyasal DengeAibleA
Grafik-1
Grafik-2
Grafik-3
Yukarıda görülen sütun grafiklerinde yeşil sütun denge kesrini (Qc), kırmızı sütun derişimler türünden denge sabitini
(K) ifade etmektedir.
be < Qe
Buna göre;
QC
Grafik-1 de sistemin dengeye ulaşabilmesi için, reaktifler yönüne hareket etmesi gerekir.
II. Grafik-2'de sistem dengededir.
III. Grafik-3 te sistemin dengeye ulaşabilmesi için geri yönlü tepkime hızının azalması, ileri yönlü tepkime hızının
artması gerekir.
yargılarından hangileri doğrudur?
A) Yalnız II
B) Yalnız III
C) I ve Ill
243
D) Il ve Il
E) I, II ve III
1234
ADEA
![3.
3- 6. soruları aşağıdaki verilen deney sonuçlarına
göre cevaplayınız.
3X(g) + 2Y(g) →→→→X3Y2(g)
Tepkimesine ait bazı deney sonuçları tablodaki gibidir.
[X], M
Tepkime Hızı M/Sn
0,01
1 x 10-4
0,02
2 x 10-4
0,01
4 x 10-4
PakN].CJ
2.15% = 445² 1215², ₁
ks t
Tepkime hız denklemi hangi seçenekte doğru veril
miştir?
bi
Deney
1
2
3
A) Hız = K[X]
CHız = K[X] [Y]
fc²
[Y], M
0,2
0,2
0,4
B) Hız = K[Y]
✅✅Q) Hız = k[X]² [Y]
EHız = K[X] [Y]²
m²
42
b=!
4. Tepkime hız sabiti k nın değeri kaçtır?
A) 100 B) 50
C) 25
D) 5
E) 1](https://media.kunduz.com/media/question/seo/raw/20230323170708499065-5229873.jpg?w=256)
Kimya
Tepkime Hızları3.
3- 6. soruları aşağıdaki verilen deney sonuçlarına
göre cevaplayınız.
3X(g) + 2Y(g) →→→→X3Y2(g)
Tepkimesine ait bazı deney sonuçları tablodaki gibidir.
[X], M
Tepkime Hızı M/Sn
0,01
1 x 10-4
0,02
2 x 10-4
0,01
4 x 10-4
PakN].CJ
2.15% = 445² 1215², ₁
ks t
Tepkime hız denklemi hangi seçenekte doğru veril
miştir?
bi
Deney
1
2
3
A) Hız = K[X]
CHız = K[X] [Y]
fc²
[Y], M
0,2
0,2
0,4
B) Hız = K[Y]
✅✅Q) Hız = k[X]² [Y]
EHız = K[X] [Y]²
m²
42
b=!
4. Tepkime hız sabiti k nın değeri kaçtır?
A) 100 B) 50
C) 25
D) 5
E) 1

Kimya
Kimyanın Temel Kanunlarıne-
1
3
2
3
7. S ve O₂ elementleri arasında SO₂ bileşiğinin olu-
şumuna ait grafik aşağıda verilmiştir.
SO3'ün kütlesi (g)
35
A)
14
Buna göre, SO, bileşiğindeki
ms
kütlece birleşme oranı
mo
3
2
B)
S'nin
20 kütlesi (g)
2
3
C)
3
elementlerin
kaçtır?
D)
3
4
E) 1
10. X
B
1
y
A
X

Kimya
Kimyasal Tepkimelerde Hesaplamalar12. Eşit mol sayısında C,H, ve O₂ gazları arasında ka-
palı bir kapta gerçekleşen;
ay
C₂(g) + 402(g) → 3CO₂(g) + 2H₂O(s)
tepkimesi sonucunda 26,4 gram CO₂ gazı oluş-
016 04
maktadır.
12
Buna göre tepkime ile ilgili aşağıdaki ifadeler-
den hangisi doğrudur? (H:1, C:12, 0:16) 44
A) Tepkimede oluşan H₂O(s) NK'da 8,96 L hacim
kaplar.
BY Tepkime başlangıcında alınan C₂H₂ ve ₂ gaz-5
Tarının mol sayıları toplamı 1 moldür.
C) Tepkimede harcanan CH, gazı 8 molekül-
gramdır.
364
40.2
Tepkime sonunda kapta bulunan maddelerin
mol sayıları toplamı 1,6 moldür.
Tepkimenin sınırlayıcı bileşeni C,H, gazıdır.
A
22,4
4.224
10 10
014
TYT Kurumsal Deneme - 4
YAYIN DENİZİ
yo
8,9%
37

Kimya
Kimyanın Temel KanunlarıX₂Y3 bileşiğinin %70'i X'tir.
Buna göre,
1. Elementlerin atom ağırlıkları oranı
7'dir.
2
II. Eşit kütlede X ve Y'den 40 g X₂Y3 elde edi-
lirken 16 g X artar.
III. 27 g XY bileşiği elde etmek için 6 g Y kulla-
nılmalıdır.
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız II
D) I ve III
C) Yalnız III
E) I, II ve III
Kimya
Kimyasal Türler ve EtkileşimlerIZING
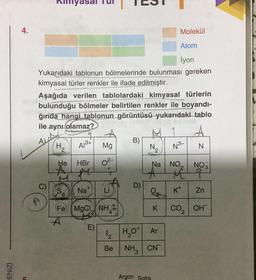
4.
LO
Molekül
Atom
İyon
Yukarıdaki tablonun bölmelerinde bulunması gereken
kimyasal türler renkler ile ifade edilmiştir.
Aşağıda verilen tablolardaki kimyasal türlerin
bulunduğu bölmeler belirtilen renkler ile boyandı-
ğında hangi tablonun görüntüsü yukarıdaki tablo
ile aynı olamaz?
ALP
A1³+
Mg
He HBr 0²-
A
H₂
2
8
Nat
Fe MgC NH
A
E)
+0*
B)
D)
N₂₂
Na
A
O
K
1₂ H₂0 Ar
Be
NH3 CN
Argon Sofra
№³-
NO₂
NO 3
M7
K+ Zn
CO2
Z
OH

Kimya
Kimyanın Temel KanunlarıKütle
b
a-
0
Buna göre,
I.
Y
III.
X
X ile Y arasında gerçekleşen tepkimeye ait kütle
zaman grafiği yukarıda verilmiştir.
10
ve !!!
20
→ Zaman
B) Yalnız II
ve b değerleri verilirse bileşiğin formülü
bulunabilir.
II. X ve Y'nin atom ağırlıkları verilirse bileşikte-
ki sabit oran bulunabilir.
a.b
b-a
yargılarından hangileri doğrudur?
A) Yalnız I
200/=
= 20
g X eklenirse artan madde olmaz.
C) Yalnız III
E) I, II ve III

Kimya
Hibritleşme ve Molekül GeometrileriBa-
A
27. X ve Y atomlarının oluşturduğu XY, molekülü ile ilgili,
1.
3 tane polar kovalent bağ içerir.
nik-
II. Her bir X-Y bağı X'in sp³ hibrit orbitali ile Y'nin s orbita-
linin örtüşmesi sonucu oluşur.
III. 2 tane ortaklanmamış elektron çifti içerir.
yargılarından hangileri doğrudur?
A) Yalnız !
B) Yalnız II
D) II ve III
C) I ve II
E) I, II ve III
