Elektrot Potansiyelleri Soruları

Kimya
Elektrot PotansiyelleriGünlük yaşantımızın vazgeçilmez bir parça-
si olan piller, kimyasal enerjiyi elektrik enerjisi-
ne dönüştürerek depolayan aygıtlardır. Geniş bir
kullanım alanına sahip olan lityum-iyon pilleri cep
telefonlarında, dizüstü bilgisayarlarda, küçük ev
aletlerinde yaygın olarak kullanılmaktadır.
11.
Buna göre, lityum-iyon pilleri ile ilgili;
1. Şarj edilerek defalarca kullanılabilirler.
II. Hafif olup, enerji yoğunlukları yüksektir.
III. Toksik (zehirli) etkiye sahip değillerdir.
yorumlarından hangileri yapılabilir?
B) Yalnız
(C) I ve'll
E) I, II ve III
A) Yalnız I
D) II ve III
DIN YAYINLARI

Kimya
Elektrot PotansiyelleriYeterince MgSO içeren sulu çözelti 5 A'lık bir akım
kullanılarak 9,65 saat elektroliz edildiğinde katotta
kaç gram Mg metali birikir?
(Mg = 24 g/mol; 1 F = 96500 C/mol e; 1 saat = 3600 s)
A) 5,4
B) 10,8
C) 21,6
D) 43,2
E) 86,4

Kimya
Elektrot PotansiyelleriQoyma 0,02mal
9. 4 L'lik CuSO4 çözeltisinden 0,04 Faradaylık akım geç-
+2-2
tiğinde,
1. Katotta 2,56 g Cu katısı birikir.X
II. Anotta NK'da 0,224 L O₂ gazı açığa çıkar. L
III. Son durumda çözeltinin pH'ı 2'dir.
yargılarından hangileri doğru olur?
(Cu: 64 g/mol, Elektron verme eğilimleri; H₂>Cu>OH > SO2)
A) Yalnız I
B) Yalnız II
C) II ve III
D) I ve III
E) I, II ve III
Orbital Yayınları
Kimya
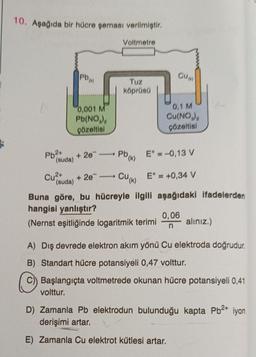
Elektrot Potansiyelleri10. Aşağıda bir hücre şeması verilmiştir.
Voltmetre
Pb²+
(suda)
Cu²+
0,001 M
Pb(NO₂)₂
çözeltisi
Pb(k) E = -0,13 V
Cu(k) E° = +0,34 V
Buna göre, bu hücreyle ilgili aşağıdaki ifadelerden
hangisi yanlıştır?
(Nernst eşitliğinde logaritmik terimi
(suda)
+2e
+ 2e
Tuz
köprüsü
-
Cu
0,1 M
Cu(NO3)2
çözeltisi
0,06
n
alınız.)
A) Dış devrede elektron akım yönü Cu elektroda doğrudur.
B) Standart hücre potansiyeli 0,47 volttur.
C)) Başlangıçta voltmetrede okunan hücre potansiyeli 0,41
volttur.
D) Zamanla Pb elektrodun bulunduğu kapta Pb²+ iyon
derişimi artar.
E) Zamanla Cu elektrot kütlesi artar.

Kimya
Elektrot PotansiyelleriNEME
₁
Cu cub
Cu²+
|
iyo
AYT/ KİMYA
9. Aşağıda kendiliğinden çalışan elektrokimyasal bir hücre
verilmiştir.
Anot
Zn (k)
0,1 M
Zn²+
(suda)
A) Yalnız I
Ag(x)
Elektrokimyasal hücre çalıştıktan sonra Ag elektrodun
kütlesinin arttığı ve hücre potansiyelinin "E" volt olduğu
gözleniyor.
0,1 M
Ag (suda)
Bu elektrokimyasal hücreyle ilgili;
1. Dis devrede elektron akımı Zn elektrottan Ag elektro-
da doğrudur.
II. Agt derişimi 1 M yapılırsa hücre potansiyeli
(E+ 0,059) V olur.
Kato
III. Her iki katyon çözeltisinin derişimi 10 katına çıkartı-
0,059
lırsa hücre potasiyeli (E+
V olur.
2
DY II ve III
ifadelerinden hangileri doğrudur?
(25 °C'de Nernst eşitliğinde logaritmik terimin katsayısı
0,059
alınacaktır; n hücre tepkimesinde aktarılan elektron
n
sayısıdır.)
B) I ve II
C) I ve III
E) I, II ve III

Kimya
Elektrot PotansiyelleriH
2
CIN
Z
HR
RENK
+4
39
8. Aşağıda lityum-iyon pilleri ile ilgili kavram haritası oluştu-
rulmuştur.
Li elektrot
katottur.
İkincil nesil pildir.
||
Lilyum-iyon MT Elektrolit
pilleri
katıdır.
Buna göre kavram haritasına aşağıdaki bilgilerden han-
gileri doğru olarak yerleştirilmiştir?
A) Yalnız I
M
B) II ve III
C) Yalnız II
D) I ve III
Lit te Li(K)
E) I, II ve III
Diğer sayfaya geçiniz.

Kimya
Elektrot PotansiyelleriÇIKMIŞ SORU
7.
@= t·+
9,65.000 5
8650.6
1.96500
965 180 ÖSYM KÖŞESİ
173700
Yeterince MgSO, içeren sulu çözelti 5 A'lik bir akım
kullanılarak 65 saat elektroliz edildiğinde katotta
kaç gram Mg metali birikir?
(Mg = 24 g/mol; 1 F = 96500 C/mol e; 1 saat = 3600 s)
A) 5,4
B) 10,8
C) 21,6
D) 43,2 E) 86,4
S
Mg +2 +2e + Mg lk)
AYT - 2019
Kimya
Elektrot Potansiyelleris
Su nove edince oren terat
Anotour.
V
Cu(k)
Kavet
0000000
Stor
Macucketpair
(pilseries)
X M Cu(NO3)2
A) Yanız il
0000000
Tuz köprüsü
D#vel
Y M Cu(NO3)2 Anot
1 yan hücre
2 yan hücre
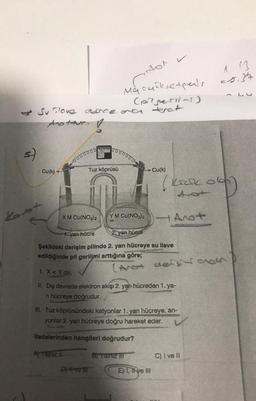
Şekildeki derişim pilinde 2. yarı hücreye su ilave
edildiğinde pil gerilimi arttığına göre;
1. X<Y dir.
II. Dış devrede elektron akışı 2. yarı hücreden 1.ya-
n hücreye doğrudur.
Cu(k)
III. Tuz köprüsündeki katyonlar 1. yan hücreye, an-
yonlar 2. yarı hücreye doğru hareket eder.
ifadelerinden hangileri doğrudur?
B) Yainiz il
(KILDL old
Ast
E) I, ve III
(Anot defisit onown
1 13
= 2.37
104)
C) I ve II
33

Kimya
Elektrot Potansiyelleri18.
Ž
Ni(K)
1M
NI(NO3)2 çözeltisi
1. kap
Ni²+ + 2e¯ → Ni
2H+
(suda)
+ 2e¯→ H₂(g)
olduğuna göre
X. Pil potansiyeli - 0,25 volttur.
PI
Pil şeması
1M
HCI çözeltisi
2. kap
► Ag(k)
D) I ve II
Eº = -0,25 V
Ni(k) | Ni²+ HH₂(g)
(suda)
(suda)
E° = 0,00 V
şeklindedir.
I. Kaptaki çözeltinin pH değeri zamanla azalır.
verilen ifadelerden hangileri yanlıştır?
A) I, II ve III
B) II ve III
C) I ve III
E) Yalnız III

Kimya
Elektrot Potansiyelleri(3
5,34
144
mgi-
me
de
5)
(6)
Cu(k)-
17de
Su love carce on teret
Anottur.!
0000000
XM Cu(NO3)2
2₁ Cindligens
Cu Curieseltpers
Tuz köprüsü
3. çözelti
2. çözelti
D#vell
0000000
Y M Cu(NO3)2
(pipelin!)
> -1,1
aren 170128
1. yan hücre
2 yan hücre
Şekildeki derişim pilinde 2. yarı hücreye su ilave
edildiğinde pil gerilimi arttığına göre;
1. X<Y dir.
II. Diş devrede elektron akışı 2. yarı hücreden 1. ya-
n hücreye doğrudur.
B) Yainiz III
z (suda)
III. Tuz köprüsündeki katyonlar 1. yan hücreye, an-
yonlar 2. yarı hücreye doğru hareket eder.
✓
Ifadelerinden hangileri doğrudur?
A) Yanız II
(suda)
Cu(k)
1. çözeltiX (suda)
(Anot defsionow
(KELD O
Ast
4941
E), Ive Ill
C) I ve II
3. kap: X(k)
06)
2. kap: Y(k)
→1. kap: Z(k)
X, Y, Z metallerinden yapılmış ve içerisinde belirtilen
Avere çözeltiler bulunan şekildeki sistemde, kaplar çözel-

Kimya
Elektrot PotansiyelleriO
3
1M X(suda)
Tuz köprüsü
X(K)→ X²+(suda) + 2e¯
Y(k)→ Y* (suda) + e¯
gişmez
Artar
1M Y(suda)
E = +0,27 volt
E° = -0,80 volt
AYDIN Yayınları
Şekildeki elektrokimyasal X - Y pilinin potansiyeli ile il-
gili aşağıdakilerden hangisi yanlıştır?
(Y₂S katısının arı sudaki çözünürlüğü çok azdır.)
A) X yarı piline aynı sıcaklıkta saf su eklenirse pil potansi-
yeli artar.
B) Y yarı piline aynı sıcaklıkta saf su eklenirse pil potansi-
yeli azalır.
C) Y yarı pilinde aynı sıcaklıkta Na₂S katısı çözünürse pil
potansiyeli artar.
D) Y yarı pilinde aynı sıcaklıkta YNO katısı çözünürse pil
potansiyeli artar.
3
AYDIN YAYINLARI
E) X yarı pilinde aynı sıcaklıkta X(NO3)2 katısı çözünürse
pil potansiyeli azalır.
yüks
erime v
lıkla yar
E) Organik
çözücül
çözünür
11. Etanol bil
liştir?
A) Renksi
B) Glikozu
elde ec
C) iyi bir g
D) Formu
59
EVArabal
12. X: CH₂-
X, Y ve
hangisi
A) Y, pri
B) X, Y
C) Z, as
D) Z, ma
EL Aynı
Z>
13. Dimetil
1. Met
II. Sim
III. Bir
yargıla
A Yalm

Kimya
Elektrot PotansiyelleriMİRAY
9.
x(K)
Anut
1 M
a+
X (suda)
1. kap
V
A) Yalnız I
Tuz köprüsü
D) II ve III
1 M
b+
(suda)
2. kap
Şekildeki elektrokimyasal pil çalışırken X
elektrotun miktarı 0,2 mol azalırken, Y elekt-
rotun kütlesi 43,2 gram artmaktadır.
Buna göre, X - Y pili ile ilgili;
1. Yb+ iyonları derişimi zamanla azalır.
=
II. a ve b iyon değerleri arasında, a 2b
ilişkisi bulunur.
Y
III. 1. kaptaki çözeltinin yarısı boşaltıldığın-
da pil gerilimi azalır. X (dzğişmez)
yargılarından hangileri doğrudur?
(X: 64, Y: 108)
B) I ve II
katut
C) I ve III
E) I, II ve III
6C 7B 8A 9B
E
a
W
E
ic
r
●
2
Z
E
r

Kimya
Elektrot Potansiyellerist
10. Aşağıda bir hücre şeması verilmiştir.
Anot
1.10-3
1.10-1
9147
Pb²+
(suda)
Pb (k)
0,001 M
Pb(NO3)2
çözeltisi
+ 2e
Cu²+ + 2e
(suda)
Voltmetre
Tuz
köprüsü
Pb₁
(k)
Cu(k)
Katot
Buna göre, bu hücreyle ilgili
hangisi yanlıştır?
(Nernst eşitliğinde logaritmik terimi
CU(K)
0,1 M
Cu(NO3)2
çözeltisi
E° = -0,13 V
E° = +0,34 V
L3
aşağıdaki ifadelerden
0,06
n
kotot
i
D'Y
alınız.)
A) Diş devrede elektron akım yönü Cu elektroda doğrudur.
B) Standart hücre potansiyeli 0,47 volttur.
Başlangıçta voltmetrede okunan hücre potansiyeli 0,41
volttur.
D) Zamanla Pb elektrodun bulunduğu kapta Pb²+ iyon
derişimi artar.
E) Zamanla Cu elektrot kütlesi artar.
12

Kimya
Elektrot Potansiyelleriin-
0,2
51-
T.
CAP
9.
Ag
V
Tuz köprüsü
04.11M AgNO
1. kap
Cu²+(suda) + 2e → Cu(k)
C
2 Ast
→ Cu
1 M CUSO 4
2. kap
E° = 0,34 V
Ag (suda) + e → Ag(k) E = 0,80 V
Yukarıdaki pil sistemine sabit sıcaklıkta aşağıdaki
işlemlerden hangisinin uygulanması pil potansiye-
lini azaltır?
(CuS nin sudaki çözünürlüğünü ihmal ediniz.)
A) 1. kaba AgNO katısı ekleyip çözmek.
kaptan H,S gazı geçirmek.
1. kaba derişimi 2 M olan AgNO, çözeltisi eklemek
2. kaba derişimi 0,5 M olan CuSO çözeltisi ekle-
mek.
E) 1. kaba bir miktar saf su eklemek.

Kimya
Elektrot Potansiyelleri8.
Aynı grupta yer alan X, Y ve Z metallerinin elektron
verme eğilimleri arasındaki ilişki X>Z>Y şeklindedir.
Buna göre aşağıdaki ifadelerden hangisi yanlıştır?
A) Metallerin yarıçapları arasındaki ilişki X > Z> Y
şeklindedir.
B) En kuvvetli indirgen X metalidir.
C) ZCI, çözeltisinin bulunduğu kaba X metali batırıldı-
ğında Z²+ iyonları indirgenir.
2
D) Z metalinden yapılmış kapta Y(NO3)2 çözeltisi sak-
lanabilir.
E) İndirgenme eğilimi en büyük olan Y²+ iyonudur.
11.
A
Kimya
Elektrot Potansiyellerit
36
27.
D) Sabit sıcaklıkta kaba bir miktar saf su eklenirse çözelti-
nin pOH değeri değişmez.
E) Sabit sıcaklıkta kaba NaOH() eklenirse Ca²+ iyonları
derişimi azalır.
Ag
1 L
Tuz köprüsü
0,25 M Ag
çözeltisi
1. hücre
+
Ag (k)
H2(g)
A) Yalnız III
0,05 MH+
çözeltisi
2. hücre
Pt
Ag+ (suda) + e- →
E° = + 0,80 V
2H+
(suda) + 2e-
E° = 0,00 V
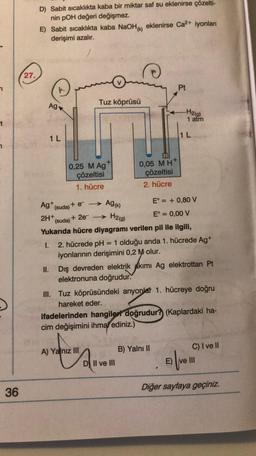
Yukarıda hücre diyagramı verilen pil ile ilgili,
-H2(g)
1 atm
1.
2. hücrede pH = 1 olduğu anda 1. hücrede Ag+
iyonlarının derişimini 0,2 M olur.
DI II ve III
L
II. Dış devreden elektrik akımı Ag elektrottan Pt
elektronuna doğrudur.
III. Tuz köprüsündeki anyonlar 1. hücreye doğru
hareket eder.
B) Yalnı II
ifadelerinden hangiler doğrudur? (Kaplardaki ha-
cim değişimini ihmal ediniz.)
C) I ve II
E) ve III
Diğer sayfaya geçiniz.
