Kimyanın Temel Kanunları Soruları

Kimya
Kimyanın Temel KanunlarıSoru 80:
Eşit kütlede Mg ve O₂ alınarak MgO elde edilirken 4 gram oksijen artmaktadır.
Buna göre başlangıçta alınan Mg miktarı kaç gramdır? (Mg:24, 0:16)
A) 16
B) 12
C) 10
D) 8
E) 6
Alg
eu
t
0₂
16
uog

Kimya
Kimyanın Temel KanunlarıÖrnek Soru 71
C3H8(g) +502(g) → 3CO₂(g) + 4H₂O(g)
tepkimesine göre, eşit mollerdeki C3H8 ve O₂ gazları tam verimle tepkimeye girerek 0,4 mol
H₂O ve bir miktar CO₂ gazları elde ediliyor.
Buna göre, aşağıdaki ifadelerden hangisi yanlıştır? (C = 12 g/mol, O = 16 g/mol)
A) Sınırlayıcı bileşen O₂ dir.
B) C3Hg den 0,4 mol artar.
C) Oluşan CO₂ nin kütlesi 13,2 gramdır.
D) Başlangıçtaki gaz karışımı toplam 0,6 moldür.
E) C3H8 gazının molce %20 si harcanmıştır.
Çözüm
3. 23 gram C₂H5OH bileşig
Normal koşullarda kaç
(C= 12 g/mol, H=1 g
4. 8,5 gram NH₂ oluştu
N₂ ve H₂ tepkimeye
(N=14 g/mol, H=1
5. Kalsiyum hidroksit
ile tam verimle et
oluşturmaktadır.
a) Tepkime der
b) 0,3 mol k
roklorik
c) 7,2 gr
yum
tepki
(H=

Kimya
Kimyanın Temel KanunlarıTEMEL KANUNLARI VE KİMYASAL HESAPLAMALAR
Örnek Soru 70
KCIO3(k) →KCI(K) +
23/1-402(9)
tepkimesine göre 147 gram KCIO3 katısının ısıtılması ile 0,9 mol O₂ gazı elde edildiğine
göre, tepkimenin verim yüzdesi kaçtır? (KCIO3 = 122,5 g/mol)
A) 10
B) 25
C) 40
Çözüm
D) 50
E) 80
Jygulama-
4NH3(9)
tepkimesi
litre NO g
tepkimey
C₂Hx(C
yakma
x kaç
23 g
No
(C

Kimya
Kimyanın Temel KanunlarıPERIŞTIRME
10. Sabit hacimli bir kapta 2 mol PCl5 ile
PCl3(g) + Cl₂(g)
PC15(g)
tepkimesi gerçekleştiriliyor.
PCI, gazının molce % 40'ı harcandığında kap-
taki toplam gaz mol sayısı kaç olur?
waula isep
A) 1,2 B) 1,4
A
C) 1,8 D) 2,4 E) 2,8
May 20
CAP
13

Kimya
Kimyanın Temel KanunlarıOrbital Yayınları
5. FeO, Fe2O3 ve Fe3O4 bileşiklerinde demir ve oksijen ele-
mentlerinin kütlelerini gösteren grafik aşağıda verilmiştir.
Demirin kütlesi
(gram)
binelis
A)
B
D)
E)
1. Bileşik
FeO
FeO
Fe2O3
ucze
Fe2O3
Fe3O4
FRL 3
anal
1. Bileşik
4
Buna göre grafikte yer alan 1., 2. ve 3. bileşiklerin for-
mülleri aşağıdakilerden hangisinde doğru olarak veril-
miştir?
2. Bileşik
Fe2O3
Fe3O4
Fe3O4
FeO
FeO
2. Bileşik
HEILS
29
3. Bileşik
06
hed
ella f
fez
Oksijenin kütlesi
(gram)
3. Bileşik
Fe3O4
Fe₂O3
FeO
Fe3O4
Fe₂O3
200
2x

Kimya
Kimyanın Temel Kanunları2.
I. CH4 + O2
II. C₂H5OH + 0₂
III. CH3OH + O₂
+ CO2 + H2O
+ CO2 + H2O
Yukarıdaki denklemlere göre eşit mollerde CH4,
C₂H5OH ve CH3OH'ı yakmak için harcanan oksijen
(02) miktarları aşağıdakilerden hangisinde doğru kı-
yaslanmıştır? (Denklemler denkleştirilecek)
A) I>II>III
B) II>III>I
+ CO2 + H2O
D) ||>1=III
E) III>I>II
C) II>I>III
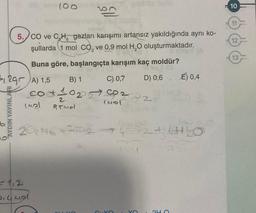
Kimya
Kimyanın Temel Kanunları29 A) 1,5
AYDIN YAYINLARI
D
100
5. CO ve C₂H gazları karışımı artansız yakıldığında aynı ko-
şullarda 1 mol CO₂ ve 0,9 mol H₂O oluşturmaktadır.
Buna göre, başlangıçta karışım kaç moldür?
Sll
Dimpl
B) 1
co +10277002
(Mal
PTMol
C) 0,7 D) 0,6 E) 0,4
IMOI
20₂46 +702 →74032 +150
101
C
C
10
11
12
13
PILI

Kimya
Kimyanın Temel Kanunları316 314 402
7. Periyodik sistemin ayni periyodunda yer alan X, Y ve Z ele-
mentlerinin birinci iyonlaşma enerjileri sırasıyla 336,314 ve
402 kkal/mol'dür.
Buna göre,
1A 2A 3A
X
Y
D) I ve III
N
4A
Y
X
5A 6A
N
kesitlerinden hangileri doğru olabilic?
A) Yalnız I
B) Yalnız III
1A 2A
X
E) II ve III
X
N
3A
C) I ve II
Y

Kimya
Kimyanın Temel KanunlarıSoru 27
Nişadır' ın (NH4CI) analizinden amonyak ve tuz ruhu
oluşmaktadır. 107 g saf nişadır' in analizinden normal
koşullarda 1,12 L tuz ruhu oluştuğuna göre nişadır'ın
% verimi kaçtır? (H: 1 g/mol, N: 14 g/mol, Cl: 35,5 g/
mol)
A) 2,5 B) 5,0 C) 7,5 D) 10 E) 12,5

Kimya
Kimyanın Temel Kanunları2NaOH(suda) + H₂SO4(suda) → Na2SO4(suda) + 2H₂O(s)
12 gram kütlece % 40 lik NaOH çözeltisi 600 mililitre H₂SO4
çözeltisi ile artansız tepkimeye giriyor.
Tepkimede kullanılan H₂SO4 çözeltisinin derişimi kaç
molardır? (NaOH : 40)
A) 1
B) 0,2
C) 0,15 D) 0,1 E) 0,01
B
160
lič
Bu

Kimya
Kimyanın Temel Kanunları39. Saf olmayan madde kullanılan tepkimelerde elde edilecek ürünün miktarı bulunurken saflık yüzdesinin de dikkate
alınması gerekir.
53
Buna göre %80 saflıkta CaCO3 içeren 50 gramlık bir karışım,
35
CaCO3(k) → CaO(k) + CO₂(g)
tepkimesine göre ayrıştığında NK'da en fazla kaç litre CO₂ gazı elde edilir?
(C:12 g/mol, O:16 g/mol, Ca:40 g/mol)
A) 5,6
B) 6,72
40
12
+48
100
45
8,8
€8,96
22,4
425
4,25
125
D) 11,2
35
Ime
E) 13,44

Kimya
Kimyanın Temel KanunlarıA
14. 0,1 mol SO2 gazıyla ilgili aşağıdaki yargılardan
hangisi yanlıştır?
(S = 32 g/mol, O = 16 g/mol, N = 6,02 - 1023)
A) Kütlesi 6,4 gramdır.
B) 1,204 1023 tane molekül içerir.
C) Normal şartlarda 2,24 L hacim kaplar.
D) 0,2 mol oksijen (O) atomu içerir.
E) 3,2 g kükürt (S) atomu içerir.
.

Kimya
Kimyanın Temel Kanunları10
B) 0,8
14 324
3016
Örnek: (1)
40 gram NaOH ve 17,6 gram CO₂
2NaOH + CO₂
Na₂CO3 + H₂O
denklemine göre tam verimle tepkimeye giriyor. 324
Bu tepkimede oluşan Na₂CO3 ün mol sayısı kaçtır?
(NaOH=40 g.mol-¹, CO₂=44 g.mol-¹)
V to
C) 0,5
$
D) 0,4
54
/E) 0,2
De
Sa
15
m
8
E

Kimya
Kimyanın Temel KanunlarıBenzinin bileşiminde bulunan oktan (C8H18) bileşiği-
nin yanma tepkimesi,
+250216CO2 + 18H₂O
2C8H18
şeklindedir.
114 g oktan yeterli miktarda oksijen ile tam verimle
yakıldığında 352 gram CO2 ve 162 gram H₂O açığa
çıkarmaktadır.
Buna göre yanma tepkimesinde harcanan O₂ gazi
kaç gramdır?
PALME
3. ÖRNEK
JASINIAYA
belirti
Buna
kullar
A) Ya
A) 76
B) 200
C) 304 D) 400 E) 476
2 (8418 + 25 0₂ 16 20₂+18/+₂00
114
+352 +162
414
5. C
Eşit kü
Timle c
bileşik
Buna

Kimya
Kimyanın Temel Kanunları9.
X ve Y elementlerinden oluşan XY3 bileşiği kütle-
ce % 60 Y içermektedir.
Buna göre,
I. XY₂ bileşiği kütlece % 50 X içerir.
II. X ve Y elementlerinin mol kütleleri
1
daki oran dir.
2
III. XY3 bileşiğinde elementlerin kütlece birleşme
mx) oranı
'my
yargılarından hangileri doğrudur?
// tür. ✓
A) Yalnız I
B) Yalnız II
D) I ve III
arasın-
7
C) Yalnız III
E) I, II ve III

Kimya
Kimyanın Temel KanunlarıE) I, II ve III
molekül formülünden
mentlerin atom sayısı
eşiğin 0,5 molünde 12
5. Organik bir bileşiğin 6 gramının tam yanmasıyla
8,8 gram CO₂ gazı ile 3,6 gram H₂O elde ediliyor.
Bileşiğin mol kütlesi 60 gram olduğuna göre
basit ve molekül formülü aşağıdakilerden han-
gisidir? (H: 1, C: 12, O: 16)
A)
B)
C)
D)
E)
Cx Hy J₂
76
Basit formül
CH₂O
C₂H₂O
CH₂O
CH₂O
C₂H₂O
1924
biy
2001
Molekül formülü
C3H603
C4H1202
CH₂O
C₂H4O2
C6H1803
₂ +4₂0
3.6
92mol
818
ID
