Koligatif Özellikler Soruları

Kimya
Koligatif Özelliklersini hesaplayınız. (60)
0,93 = 1,86. x=ar
aš
ar
2,5 mol
3) Saf suyun 27°C'de buhar basıncı 55 mmHg'dır. Buna göre,
27°C'de 720 g saf suya 117 g NaCl ilave edilip çözülürse çözeltinin
g
buhar basıncı kaç mmHg olur? H20= 18, NaCl=58,5)
(50)
home and
hos 50
4
- reser 4 chall
4) Eşit mol sayısında etil alkol ve su içeren bir karışımın
20°C'deki buhar basıncını hesaplayarak saf suyun buhar basıncı
ile karşılaştınız. (20°C'de Ps= 18mmHg, pº
etil alkoi= 44mmHg)
(31)
1, 18t 1,44

Kimya
Koligatif Özellikler3. Aşağıdaki grafikte suyun normal donma noktası referans alı-
narak, iki farklı sulu çözeltinin donma noktasındaki düşüşün
(at) derişime bağlı olarak değişimi verilmiştir.
0,2
0.1
0,3
0
Derişim (mol/L)
-a
X
-2a
Y
.
At(°C)
Buna göre X ve Y ile belirtilen maddeler
x
Y
1. K2SO4
AlBrz
Mg(NO3)2
II. KCI
NaCl
III. MgCl2
hangileri olabilir?
A) Yalnız!
B) Yalnız II C) I ve II
E) II ve III
D) I ve III

Kimya
Koligatif Özellikler18. Suda moleküler halde çözünen ve uçucu olmayan saf X mad-
desinin 18 gramının 520 gram saf suda tamamen çözünmesi
sağlanıyor.
Oluşan çözeltinin 1 atmosfer basınç altındaki kaynama Si-
caklığı 100,2 °C olduğuna göre X maddesinin mol kütlesi
kaç gramdır?
(Su için kaynama sıcaklığı yükselme sabiti (K) = 0,52 °C/m'dir.)
A) 40
B) 45
C)
90
D) 120
E) 180

Kimya
Koligatif Özellikler11
1s
3
n=1
katman ve alt katmanların enerji düzeyleri grafiktek
gibidir.
II. Temel hal elektron dizilimindem, değeri +1 olan top-
3
lam elektron sayısı 5 dir.
III. Periyodik sistemin 4. periyot 6B grubu elementidir.
yargılarından hangileri doğrudur?
B) Yalnız II
C) I ve II
A) Yalnız!
D) I ve III
E) I, II ve III
1
}
16. 2 kg saf suda 1 mol Al(NO3)3 tuzunun çözülmesiyle elde
edilen çözeltinin 1 atmosfer basınçta kaynamaya başla-
ma sıcaklığı saf suyunkinden 1,04°C yüksek oluyor.
Buna göre, 1 atmosfer basınçta 1 kg saf suda kaç
mol KNO, tuzu çözülürse çözeltinin kaynamaya baş-
lama sıcaklığı saf suyunkinden 3,12°C yüksek olur?
A) 2
B) 3 C) 4 D) 6 E) 12
1
0
Diğer sayfaya geçiniz.

Kimya
Koligatif Özellikler6.
85 gram NaNO, katısı 1000 gram suda çözülüyor.
Bu çözeltinin 1 atm basınçtaki kaynama sıcaklığı kaç
85
elmoc dir?
s
(NaNO3 = 85 g/mol, Kk = 0,52 °C/molal)
B) 100,52
C) 100,78
A) 100,26
D) 101,04
E) 102,08
0,52

Kimya
Koligatif Özelliklerntol
Uçucu olmayan saf bir madde saf bir sivida
çözündüğünde sivinin buhar basıncı düşer.
Sivinin buhar basıncı karışımdaki mol kes-
ri ile saf haldeki buhar basıncının çarpimin-
dan bulunur.
A sivisi ile hazırlanan bir çözeltide,
PA = PÅ XA
A
PA: Sivinin çözeltideki buhar basıncı
PÅ: Sivinin aynı sıcaklıkta saf haldeki bu-
har basıncı
ny
XA: Sivinin çözeltideki mol kesri
nteop
:
720 gram glikoz(C.,.) 360 gram suda
çözündugunde çözeltinin 25°C'deki bu-
har basıncı kaç mmHg olur?
(C, H, O, 180, HẠO: 18, 25°C de PHÚo 24 mmHg)
C6H120g: H,0
A) 16 B) 18 C) 20 D) 24 E) 26
080

Kimya
Koligatif Özellikler150 g su
45 g tuz
100 g su
60 g su
20 g tuz
1
II
III
Yukarıdaki kaplarda bulunan maddelerin
donma noktaları ve kaynama noktaları
arasındaki ilişki aşağıdakilerden hangi-
sinde doğru olarak verilmiştir?
(X tuzunun çözünürlüğü 30 g X/100 g su)
Donma noktası
A)
B)
C)
D)
E)
1>Il > III
1 = I1 = III
HIT > I > II
1 = III > II
Il > I = III
Kaynama noktası
ill > li >|
1 = Il = III
III > | > 11
I> 1 = III
1 = III > II

Kimya
Koligatif Özellikleriy
ak
6.
102
S1, 18
Su için kaynama noktası yükselme sabiti (KK)
0.52 °C/molal'dir.
Su için donma noktası alçalma sabiti (Kd)
1,86 °C/molal'dir.
NaCl tuzu ile hazırlanan bir çözeltinin deniz seviyesin-
de kaynama noktası ile donma noktası arasındaki si-
caklık farkı 102,38 °C olduğuna göre NaCl çözeltisinin
derişimi kaç molaldir?
Orbital Yayınları
A) 0,1
B) 0,5
C) 1
D) 2
E) 5
Kimya
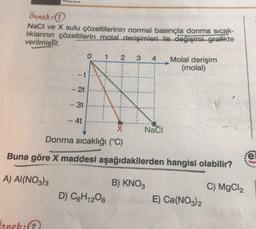
Koligatif ÖzelliklerS.
Örnek:
NaCl ve X sulu çözeltilerinin normal basınçta donma sicak-
liklarının çözeltilerin molal derişimleri ile değişimi grafikte
verilmiştir.
0
2
Molal derişim
(molal)
- t
1
3
4
-
- 2t
1
-30
NE
- 4t
Naci
Donma sıcaklığı (°C)
Buna göre X maddesi aşağıdakilerden hangisi olabilir?
:e
Yoy
A) AI(NO3)3
B) KNO3
D) C6H1206
C) MgCl2
E) Ca(NO3)2
Orneb:

Kimya
Koligatif ÖzelliklerFEN BİLİMLERİ
A
18.
Çözücü ve çözüneni uçucu olan çözeltilerde çözeltinin
buhar basinoi, çözeltideki çözücü ve çözünenin buhar ba-
sinplan toplamina eşittir.
Ahmet. 1 °C sıcaklıkta glikola (etandiol
, CH (OH),) su ile
karştırarak buhar basıncı 99,1 mmHg olan bir çözelti elde
ediyor.
Buna göre, Ahmet'in oluşturduğu karışımda suyun mol
kesrl kaçtır?
(t°C sıcaklıkta buhar basınçları su ve glikol için sırasıyla
110 mmHg ve 1 mmHg'dir.)
A) 0,1 B) 0,2 C) 0,3 D) 0,8 E) 0,9
111-997
![8,9 g sakkaroz (C12H220,-) 34,0 g suda çözülerek bir çözel.
ti hazırlanıyor. Çözeltinin kaynama noktasını hesaplayınız
(H: 1 g/mol, C: 12 g/mol, O: 16 g/mol, su için Kk = 0,51 °C]m).
Elektrolit olmayan veya](https://media.kunduz.com/media/question/seo/raw/20220329203045475931-2258363_eboWcx9QL.jpg?w=256)
Kimya
Koligatif Özellikler8,9 g sakkaroz (C12H220,-) 34,0 g suda çözülerek bir çözel.
ti hazırlanıyor. Çözeltinin kaynama noktasını hesaplayınız
(H: 1 g/mol, C: 12 g/mol, O: 16 g/mol, su için Kk = 0,51 °C]m).
Elektrolit olmayan veya

Kimya
Koligatif Özellikler3
12. Saf X Sivisina ait sıcaklık-zaman grafiği Şekil 1'deki
gibidir.
Sıcaklık (°C)
Sıcaklık (°C)
t2
Zaman
→ Zaman
Şekil 1
Şekil 2
Buna göre X Sivisina,
siviyi yükseltinin daha az olduğu bir ortama götürmek,
th Sivi miktarını artırmak,
V. isitici gücünü artırmak
işlemlerinden hangileri uygulanırsa Şekil 2'deki grafik
elde edilebilir (ty <t2)
A) Yalnız!
B) Yalniz il
)
C) Yalnız III
C)
D) I ve II
En fem

Kimya
Koligatif Özellikler4.
20°C sıcaklıkta 0,4 mol benzen ve 0,8 mol toluen
sivilarının birbiri içerisinde çözünmesi sonucu bir çö-
zelti hazırlanıyor.
Buna göre oluşan çözeltinin aynı sıcaklıktaki bu-
har basıncı kaç mmHg'dir?
(20°C'de pº 78 mmHg ve PO
21 mmHg)
benzen
toluen
A) 28
B) 33
C) 40
D) 59
E) 60

Kimya
Koligatif ÖzelliklerKutlece
kutiece
950 Naci
20 Naci
sulu çözeltisi
sulu çözeltisi
1. Bölme
2. Bölme
Şekildeki gibi yarı geçirgen zar ile ayrılmış sistem
ile ilgili;
1. Osmoz olayı gerçekleşir.
II. 1. bölmeden 2. bölmeye su geçişi olur.
III. Zamanla 2. bölmedeki sıvı yüksekliği azalır.
yargılarından hangileri doğrudur?
A) Yalnızl
C) I ve II
B) Yalnız 11
E) I, II ve III
D) I ve III

Kimya
Koligatif Özellikler9. Bir çözeltinin aynı ortamda donmaya başlama te
MAVİ HUZ
TESTI
saf suyunkinden daha düşük ise saf suya,
azar azar
scanor
Il etil alkol,
klerden
1
Süzme ile ay
1 Heterojen
I daha soğuk bir su
maddelerinden hangileri tek başına eklenmiş olabilir
B) I ve II
Kati-SIVIL
A) Yalnız!
D) Il ve III
C) Yalnız
NI. Bileşenler
yargılanındar
E) 1, Wve in
10. Çözeltinin derişimine bağlı özelliklere koligatiile
A) Yalnız!
denir
.
C
Buna göre, aşağıdakilerden hangisi koligatif özel
ile ilgili değildir?

Kimya
Koligatif Özellikler10. Antifriz, temel olarak motorun ve motor bağlantılarının so-
ğutulmasında kullanılan suyun donmasını engelleyen si-
vidir. Antifriz eklenmiş soğutma suyunun çalışabildiği en
düşük sıcaklığa koruma sıcaklığı adı verilir.
Koruma
Antifriz
Su
Sıcaklığı (°C) (Hacimce %) (Hacimce %)
-40
100
-27
0
40
-4
80
20
-18
60
-9
40
60
20
80
Su ve antifiriz sivisinin derişimine bağlı olarak koruma si-
caklığının nasıl değiştiğini gösteren bir tablo verilmiştir.
Bu tabloya göre;
1. Donma sıcaklığı derişime bağlı değişen bir özelliktir.
11. Antifriz derişimi arttıkça karışımın koruma sıcaklığı artar.
III. 1 L motor soğutma suyuna 1,5 L antifriz eklendiğinde
koruma sıcaklığı -18 °C olur.
yargılarından hangilerine ulaşılabilir?
A) Yalnız II
B) I ve il
C) I ve Ill
D) II ve III
E) I, II ve III
