Koligatif Özellikler Soruları

Kimya
Koligatif Özellikler26
1000 gram suda 1 mol C6H₁2O6 çözündüğünde 1 atmosfer
basınçta suyun kaynamaya başlama sıcaklığı 100, 52 °C
oluyor.
Buna göre, 500 gram suda 1 mol KNO3 çözündüğünde
oluşan çözelti 1 atmosfer basınçta kaç °C de kayna-
maya başlar?
A) 101,04
D) 102,60
B) 101,56
C) 102,08
E) 103,58
Çözünürlük
(x0/1000 su

Kimya
Koligatif ÖzelliklerÖrnek
2 tanecik
0,2 M NaCl sulu çözeltisinin donmaya başlama sıcaklığı -4a °C tır.
Aynı ortamda 0,1 M XCI çözeltisinin donmaya başlama sıcaklığı -3a °C olduğuna göre "n" kaçtır?
AId=- kd. m...its.
42
-30- 2
11. SINIF
Q2
0,1- (1+0)
....
z 0,3
PRA

Kimya
Koligatif Özellikler25. Sabit hacimli kapta 4,6 gram CH, ve 12.5 gram 50,
gazlarının toplam basinci 4 atm'dir.
Buna göre, CH, ve SO, gazlarının kısmi basınçları
aşağıdakilerin hangisinde doğru verilmiştir?
(CH, 16 g/mol, 50, 64 g/mol)
Po, (atm)
A)
B)
C)
D)
E)
Po(atm)
1.2
2.4
0.8
1,6
2,8
2.8
16
3.2
24
1.2

Kimya
Koligatif Özellikler8. Aşağıdaki tabloda derişimleri belirli bazı sulu çözeltiler
ve bu çözeltilerin aynı dış basınçta donmaya başlama
sıcaklıkları verilmiştir.
Çözelti
1 molal C6H12O6
1 molal X
Donmaya başlama
sıcaklığı (°C)
B) KNO3
D) AI(NO3)3
-2t
Buna göre, X maddesi aşağıdakilerden hangisi ola-
bilir?
A) NaCl
-6t
E) CaCl2
C) NH₂NO3
Kimya
Koligatif Özellikler29.
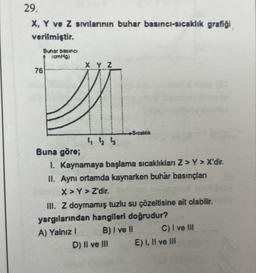
X, Y ve Z sıvılarının buhar basıncı-sıcaklık grafiği
verilmiştir.
Buhar basıncı
(cmHg)
X Y Z
A
442 4
76
Sıcaklık
Buna göre;
1. Kaynamaya başlama sıcaklıkları Z>Y > X'dir.
II. Aynı ortamda kaynarken buhar basınçları
X>Y > Z'dir.
III. Z doymamış tuzlu su çözeltisine ait olabilir.
yargılarından hangileri doğrudur?
A) Yalnız I
B) I ve II
D) II ve III
C) I ve III
E) I, II ve III

Kimya
Koligatif ÖzelliklerKoligatif özellikler, çözünenin cinsine bağlı olmayıp yal-
nızca çözeltide bulunan taneciklerin derişimine bağlıdır
ve taneciklerin molekül, anyon veya katyon oluşların-
dan bağımsızdır.
0,4 mol
NaCl
1L su
0,3 mol
şeker
1L su
Buna göre yukarıda verilen kaplardaki çözeltilerin
aynı ortamdaki kaynama noktalarının eşit olabil-
mesi için II. çözeltiye eklenmesi gereken şeker
(C6H₁2O6) miktarı kaç moldür?
A) 0,1 B) 0,2 C) 0,3
D) 0,4 E) 0,5
1
1
1
1
1
1
1
I
1
1
1
I
1
1
1
1
I

Kimya
Koligatif Özellikler12.
2 molal KNO3 çözeltisinin (100 + 2a)°C sıcaklıkta kayna-
dığı bir ortamda 1 molal MgCl₂ çözeltisi kaç °C sıcaklıkta
kaynar?
A) 100+
3a
2
D) 100+
B) 100+ a
5a
2
C) 100+ 3a
E) 100+ 3a
4
11SB01/KIMYA/A SERİSİ

Kimya
Koligatif Özellikler6.
~
2500 gram suda 171 gram Al₂(SO4)3 katısı çözünmesi ile
oluşan çözeltinin normal donma noktası kaç °C'dir?
(O: 16, Al: 27, S: 32) (Su için K = 1,86°C/m)
A) -0,93
B)-1,86
D) -5,58
C) -2,79
E) -8,37

Kimya
Koligatif Özellikler5. Bir miktar Fe2(SO4)3 katısının 600 gram suda
çözünmesiyle oluşan çözeltinin 1 atm deki donmaya
başlama sıcaklığı -9,3 °℃ dir.
4
Buna göre, çözünen Fe₂(SO4)3 kütlesi kaç gramdır?
= 400 Kd = 1,86 °C/m)
B) 240
C) 200
(Fe2(SO4)3
A) 400
3,72
F-1.4
D) 180
E) 160
w
Kimya
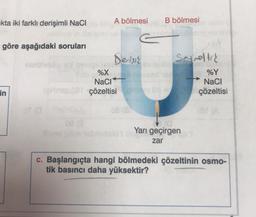
Koligatif Özelliklerkta iki farklı derişimli NaCl
göre aşağıdaki soruları
ninblasög
in
A bölmesi
Derisik
%X
NaCl
çözeltisi pr
B bölmesi
Seyreltic
Yarı geçirgen
zar
%Y
NaCl
çözeltisi
→
c. Başlangıçta hangi bölmedeki çözeltinin osmo-
tik basıncı daha yüksektir?

Kimya
Koligatif Özelliklergram
nay-
bulu-
CI 160
1.
#
TEST 11
Bir çözeltinin kaynama noktasındaki
yükselme AT = K.miyon bağıntısı ile
bulunabilir.
AT = Kaynama noktasındaki yükselme
K= Suyun kaynama noktası yükselme
sabiti
msiyon
KAZANIMLARI
= Toplam iyon molalitesi
Buna göre 2 kg suda 2 mol NaBr çözün-
düğünde oluşan çözelti normal koşullar-
da kaç °C'de kaynamaya başlar?
(Su için K = 0,52 °C-m-¹)
A) 103,12
B) 102,6
D) 101,04
C) 102,08
Düzey 1
E) 100,52
Kolig
4.
10

Kimya
Koligatif Özellikler8. Aşağıdaki grafikte, normal basınçta suyun
donma noktasındaki değişimin (AT), çözelti
derişimlerine (M) bağlı olarak değişimi veril-
miştir.
0
-a
-2a
-3a
2
X
A) Ca(NO3)2
NaCl
C) NaNO3
SISTOLE
D) CaBr₂
asaul
E) C₂H5OH
3
C6H12O6
X
AT d
Buna göre X ve Y çözeltileri aşağıdakiler-
den hangisi olabilir?
→Derişim (mol/L)
Y
KCI
Ca(NO3)2
AICI3
AI(NO3)3
AICI 3
(8

Kimya
Koligatif Özellikler12. Dış basıncın 1 atmosfer olduğu ortamda saf etil alkolün
kaynama noktası 78°C ve saf suyun kaynama noktası
ise 100°C dir.
Buna göre, saf etil alkol ve saf su ile ilgili aşağıdaki
yargılardan hangisi yanlıştır?
yanakonuyun çal
A) Saf suyun molekülleri arasındaki çekim kuvveti saf V
etil alkolünkinden güçlüdür.
B) Oda koşullarında saf etil alkolün buhar basıncı saf V
suyunkinden büyüktür.
C) Diş pasincin 0,8 atmosfer olduğu ortamda saf suyun x
kaynama sıcaklığı 100°C den yüksektir.
-De
D) Dış basıncın 1 atmosfer olduğu ortamda saf etil
alkolün 78°C deki buhar basıncı, saf suyun 100°C
deki buhar basıncına eşittir.
E) Her ikisinin de sıcaklıkları 25°C den 50°C ye yük-
seltilirse buhar basınçları artar.

Kimya
Koligatif Özelliklergeçerlidir.
de çözün-
1, donma
ncı artar.
mesi
an bir katı
kaynama-
ş basınç-
ktasından
(doyma-
başladığı
ama nok-
ma nok-
r. Bu de-
maddenin
öntemine
se: Bir sı-
inca eşit
Arı bir si-
si buhar
Iduğu si-
n bir katı
azalaca-
basıncı-
cin çözel-
üksek bir
kir. Kısa-
aklığı arı
2. Aşağıdaki çözeltiye aynı sıcaklıkta hacim
değişmeden bir miktar KCI katısı eklenip çö-
zünüyor.
Na* iyon derişimi
değişmez.
Aynı
sıcaklıkta
çözeltinin
buhar basıncı
azalır.
V
CI iyonları mol sayısı
artar.
0,5 molal
1 L NaCl
B) II
sulu
çözeltisi
Çözeltinin
donmaya
başlama
sıcaklığı
artar.
Çözeltinin aynı dış
basınçta kaynamaya
başlama sıcaklığı yükselir.
IV
Buna göre verilen bilgilerden hangisi
yanlıştır?
AYT
Ⓒ DIV EXV
C) III
D)
MIRAY YAYIN
4.

Kimya
Koligatif Özellikler4. X, Y ve C6H12O6 bileşiklerinin sulu çözel-
tilerinde derişime bağlı olarak donmaya
başlama sıcaklığındaki değişim aşağıda
ki grafikte gösterilmiştir.
0,1
0,3
T
-2t
-3t
X Y
Donma noktası (°C)
Derişim (mol.L-1)
C6H12O6
Buna göre;
1. X maddesi, CaCl₂ olabilir.
II. Y maddesinin sulu çözeltisi elektriği iletir.
H. Eşit derişimli çözeltilerinde aynı ortam-
da kaynamaya başlama sıcaklığı en dü-
şük olan X'tir.
yargılarından hangileri doğrudur?
A) Yalnız I B) Yalnız II
D) I ve II
G) Yalnız III
E) I ve !!!

Kimya
Koligatif ÖzelliklerKAZANIM TESTI 6
14. Organik bir bileşiğin 0,4 molü benzen sivisinda mole-
küler hâlde tamamen çözünüyor. Elde edilen çözeltinin
kaynamaya başlama sıcaklığı saf benzeninkinden 20,8
°C daha yüksek olarak ölçülüyor.
Buna göre organik bileşik kaç kg benzen SIVISında
çözünmüştür? (Benzen için K: 2,6 °C/m)
A) 20
C) 12
D) 8
B) 16
E) 4
0,4 =8
18. A
