Tepkime Hızını Etkileyen Faktörler Soruları

Kimya
Tepkime Hızını Etkileyen FaktörlerM- I
100
d>
0,5 =
old
n=1
8. 0,5 molarlık 2 litre HNO, sulu çözeltisine bir miktar
Na2CO3(k) eklendiğinde,
2HNO3(suda) + Na2CO3(k) →
2NaNO3(suda) + CO2(g) + H2O(s) AH<0
denklemine göre tepkime gerçekleşiyor.
Bu sisteme aşağıdakilerden hangisi tek başına yapıldı-
ğında tepkimenin başlangıç hızı değişmez?
A) 0,1 molarlık HNO3 çözeltisi eklemek
B) H2O(s) eklemek
C) Sıcaklığı düşürmek
D) KOH(k) eklemek
E) 0,5 molarlık 1 litre HNO3 çözeltisi ilave etmek

Kimya
Tepkime Hızını Etkileyen Faktörler19. Endotermik bir tepkimeye sabit sıcaklıkta uygun bir
katalizör eklendiğinde tepkimenin;
1. aktifleşme enerjisi,
II. entalpi değişimi değeri,
III. basamak sayısı
e
niceliklerinden hangilerinde değişim gözlenebilir?
A) 1, Il ve Ill
B) I ve II
C) Il ve Ill
D) Yalnız E) Yalnız III
vol
n

Kimya
Tepkime Hızını Etkileyen Faktörler22. Aşağıdaki kapta H,S, O, H,O ve So, gazları sabit ba-
sinçli kapta dengededir.
24.
ideal piston
24,90) 420,60) = 24,09)+ 250,01 +
2H S+
P2(+ Q
AH < 0
Buna göre, dengedeki sistemle ilgili aşağıdaki ifa-
delerden hangisi yanlıştır?
A) Sabit hacim ve sıcaklıkta SO, eklenirse H.S mik-
tarı artar.
Sabit hacimde kap ısıtılırsa SO, miktarı azalır.
C) Sabit hacimde katalizör eklenirse oluşan H2O mik-
tarı azalır.
Lo Sabit sıcaklıkta piston yukarı çekilirse H, S mikta-
ri artar.
21221321
E) Kaptan sabit hacim ve sıcaklıkta O, çekilirse SO2
miktarı azalır.
37

Kimya
Tepkime Hızını Etkileyen FaktörlerX
10. Katalizör ile ilgili olarak,
* Hiz sabiti k'nın değerini değiştirir.
Hi Tepkimenin yönünü değiştirir.
11. Başlaması mümkün olmayan bir tepkimeyi başlatamaz.
ifadelerinden hangileri yanlıştır?
A) Yalnız!
B) Yalnız II
C)Yalniz III
D) I ve II
E) Ilye 111
Kimya
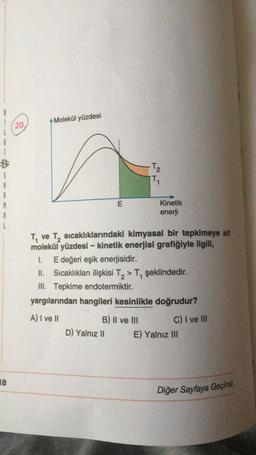
Tepkime Hızını Etkileyen FaktörlerMolekül yüzdesi
(20.
6
B
$
-T₂
TO
E
Kinetik
enerji
A
Tve
ve T, sıcaklıklarındaki kimyasal bir tepkimeye ait
molekül yüzdesi - kinetik enerjisi grafiğiyle ilgili,
1. E değeri eşik enerjisidir.
Sıcaklıkları ilişkisi T, > T, şeklindedir.
III. Tepkime endotermiktir.
yargılarından hangileri kesinlikle doğrudur?
A) I ve II
B) II ve III
C) I ve III
D) Yalnız II E) Yalnız III
18
Diğer Sayfaya Geçiniz

Kimya
Tepkime Hızını Etkileyen FaktörlerTepkime /
6 IP
3
Mg(k) + 2HNO3(suda) Mg(NO3)2(suda) + H2(9)
tepkimesine göre 2,4 gram Mg ve 200 mL 2M HNO3
çözeltisinin tam verimle tepkimesinden elde edilen H2
gazinin normal koşullardaki hacminin zamanla deği-
şimi grafik-1 deki gibidir.
AVH₂(L)
VH (L)
4,48
2,24
50 Zaman (s)
20 Zaman (s)
Grafik-2
Grafik-1
Buna göre, grafik - 2'yi elde etmek için;
1. katalizör kullanmak ve sıcaklığı artırmak,
II. Mg miktarini v sicaklığı artırmak,
III. Mg katı yüzeyini ve HNO3 çözeltisinin molar
derişimini artırmak
işlemlerinden hangileri tek başına yapılabilir?
(Mg:24)
A) Yalnız ! B) Yalnız II C) Yalnız III
D) I ve III
E) II ve III
CAP

Kimya
Tepkime Hızını Etkileyen FaktörlerAYT
15.
Derişim
Eşik enerjisi
→ Zaman
Yukarıda verilen tanecik sayısı-kinetik enerji grafiği
ile ilgili olarak aşağıdakilerden hangisi yanlıştır?
A) T₁ sıcaklığında eşik enerjisini geçen tanecik sayısı
daha fazladır.
B) T₂ sıcaklığında taneciklerinin ortalama kinetik ener-
jileri daha küçüktür.
T₁ sıcaklığında aktivasyon enerjisi daha fazladır.
D) T, sıcaklığında birim zamanda oluşan aktifleşmiş
kompleks sayısı daha fazladır.
E) T₂ sıcaklığında tepkime hızı daha küçüktür.
T₂
17. O
![15. 2XO(g) + F₂(g) →→→ 2XOF(g) tepkimesinin hız eşitliği
hiz-k[XO] [F₂] dir.
Bu tepkime için aşağıdaki mekanizma veriliyor.
1. XO(g) + F₂(g)
-
Vavas
XOF(g) + F(g)
2. XO(g) + F(g) →→→→→ XOF(g)
hilli
Buna göre, tepkimeyle ilgili aşağıdakilerden hangisi
yanlıştır?
✓
tepkimede ara üründür.
Mekanizmadaki 1. basamak 2. den daha yavaştır.
C) Net tepkime 1. basamaktan daha hızlı yürür.
D) XO(g) derişimi iki katına çıkarılırsa birim hacimdeki
molekül sayısı ve saniyedeki XO - F₂ çarpışma sayısı
iki katına çıkar. (Sıcaklık sabit)
Hem XO hem de F2 derişimleri iki katına çıkarılırsa hız
sabiti ((k) değişmez. (Sıcaklık sabit)
yavas
hızlı
6715
24
eis
19/2
18](https://media.kunduz.com/media/question/seo/raw/20220501154657445554-3363912_KXoCkyOa8.jpeg?w=256)
Kimya
Tepkime Hızını Etkileyen Faktörler15. 2XO(g) + F₂(g) →→→ 2XOF(g) tepkimesinin hız eşitliği
hiz-k[XO] [F₂] dir.
Bu tepkime için aşağıdaki mekanizma veriliyor.
1. XO(g) + F₂(g)
-
Vavas
XOF(g) + F(g)
2. XO(g) + F(g) →→→→→ XOF(g)
hilli
Buna göre, tepkimeyle ilgili aşağıdakilerden hangisi
yanlıştır?
✓
tepkimede ara üründür.
Mekanizmadaki 1. basamak 2. den daha yavaştır.
C) Net tepkime 1. basamaktan daha hızlı yürür.
D) XO(g) derişimi iki katına çıkarılırsa birim hacimdeki
molekül sayısı ve saniyedeki XO - F₂ çarpışma sayısı
iki katına çıkar. (Sıcaklık sabit)
Hem XO hem de F2 derişimleri iki katına çıkarılırsa hız
sabiti ((k) değişmez. (Sıcaklık sabit)
yavas
hızlı
6715
24
eis
19/2
18

Kimya
Tepkime Hızını Etkileyen FaktörlerAyn miktarda madde kullanılarak T, ve T, sıcaklıkla-
ninda gerçekleştirilen bir tepkimede moleküllerin kine-
tik enerjilerinin dağılımı grafikte verilmiştir.
Molekül sayısı Sıcaklık T₁
Sıcaklık = T₂
Kinetik enerji
Buna göre tepkime ile ilgili,
&
sıcaklığında birim zamanda oluşan ürün mikta-
ri daha fazladır.
sıcaklığında aktif komplekslerin potansiyel ener-
jisi fazladır.
T₁ ve T₂ sıcaklıklarında farklı mekanizma üzerin-
den yürür.
ifadelerinden hangileri doğrudur?
A) Yalnız T
B) I vell
C) I ve III
D) II ve III
Eşik enerjisi
E), 11 ve III

Kimya
Tepkime Hızını Etkileyen FaktörlerA
0,1 M
2lt
HCI
0,2 M
1lt
HCI
C
Deneylerle Hız Hesabı - Hız Bağı
B
Yandaki dört kapta, farklı
derişim ve hacimlerde HCI
çözeltileri vardır.
0,1 M
3lt
HCI
0,2 M
2lt
HCI
Bu kaplara sırasıyla,
A Kabina
B Kabina
C Kabina
D Kabina
ilave edilerek,
Zn +2HCI (suda)
ZnCl +H
2(suda) 2(g)
tepkimesi gerçekleştiriliyor. Buna göre kaplardaki tep-
kime hızlarını kıyaslayınız.
A) D>C>A>B B) A>B>C>D
CA=D>B=C
D
► 0,1 mol Zn
tozu
► 0,1 mol Zn
teli
(k)
► 0,1 mol Zn teli
(k)
► 0,1 mol Zn
tozu
D) B>C>A>D (E) D>A>C>B
DA)C>3

Kimya
Tepkime Hızını Etkileyen FaktörlerTEPKIMELERDE HIZ
8. Tepkime hızı ile ilgili aşağıdaki ifadelerden hangisi
yanlıştır?
A) Bir kimyasal tepkimenin hızı tepkimeye giren mad-
delerin birim zamandaki derişimlerindeki azalma ile
ölçülebilir.
V=n. R.T
B) Pistonlu bir kapta gerçekleşen tepkimeye reaktif ila-
vesi, tepkime hızını arttırabilir ya da azaltabilir.
C) Reaktifleri molekül yapılı olan tepkimeler genellikle
yavaş tepkimelerdir.
DAktifleşme enerjisi büyük olan tepkimeler zıt yüklü
iyonlarla gerçekleşen tepkimelere göre daha hızlıdır.
E) Bir kimyasal tepkimenin hızı, tepkimeye giren mad-
delerin etkin çarpışma sayısına bağlıdır.
1B 2B
3D
4C 5C
Kimya
Tepkime Hızını Etkileyen Faktörler21221336
0
tepkimelerinden
hangileri standart koşu
gerçekleştirilirken sürekli enerjiye ihtiyacı vardır?
(₁H, N)
Yalnız II
L
B) I ve II
C) I ve III
D) II ve III
E) I, II ve III
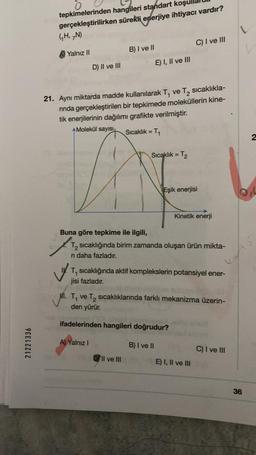
21. Aynı miktarda madde kullanılarak T₁ ve T₂ sıcaklıkla-
rında gerçekleştirilen bir tepkimede moleküllerin kine-
tik enerjilerinin dağılımı grafikte verilmiştir.
Molekül sayısı Sıcaklık = T₁
Sıcaklık = T₂
Eşik enerjisi
Kinetik enerji
Buna göre tepkime ile ilgili,
T₂ sıcaklığında birim zamanda oluşan ürün mikta-
ri daha fazladır.
1
T₁ sıcaklığında aktif komplekslerin potansiyel ener-
jisi fazladır.
Mi. T₁ ve T₂ sıcaklıklarında farklı mekanizma üzerin-
den yürür.
ifadelerinden hangileri doğrudur?
A) Yalnız I
B) I ve II
C) I ve III
Il ve III
E) I, II ve III
36
2

Kimya
Tepkime Hızını Etkileyen FaktörlerL
C
18. Bir tepkimede girenlerden ürünlere alternatif bir yol
oluşturarak tepkime mekanizması değiştiren madde-
lere katalizör denir.
Buna göre katalizörlerle ilgili,
Tepkime verimini artırırlar.
Tepkime entalpisini değiştirirler.
III. Tepkimenin aktif kompleksinin türünü değiştirirler.
ifadelerinden hangileri doğrudur?
B) Lve 11
CUI ve III
A) Yalnız III
E) I, IL ve 111
D) II ve III

Kimya
Tepkime Hızını Etkileyen Faktörler20. Sabit hacimli kapalı bir kapta,
X(9) 2Y(g) AH > 0
g=
tepkimesi belirli bir sıcaklıkta dengededir.
Sıcaklık artırıldığında kapta meydana gelen değişimler
ile ilgili aşağıdaki ifadelerden hangisi yanlıştır?
A) İleri tepkime hızı artar.
B) Geri tepkime hızı azalır.
C) Toplam basınç artar.
D) Denge sabitinin değeri artar.
3
E) X gazının mol sayısı azalır.

Kimya
Tepkime Hızını Etkileyen Faktörler11
Su
NaOH
çözeltisi
Yukandaki kapalı kaptaki beherlerde saf su ve
NaOH çözeltileri bulunmaktadır.
Bir süre sonra beherdeki sıvılar ile ilgili,
1. Su bulunan kaptan NaOH çözeltisi bulunan
kaba madde geçişi olur.
Il. NaOH çözeltisinin derişimi azalır.
III. Osmoz olayı gerçekleşir.
yargılarından hangileri doğru olur?
A) Yalnız!
B) Yalnız II
C) I vell
D) I ve III
E) I, II ve III

Kimya
Tepkime Hızını Etkileyen Faktörler20. Sabit hacimli kapalı bir kapta,
X(g) = 2Y(g) AH > 0
tepkimesi belirli bir sıcaklıkta dengededir.
Sicaklık artırıldığında kapta meydana gelen değişimler
ile ilgili aşağıdaki ifadelerden hangisi yanlıştır?
A) İleri tepkime hızı artar.
B) Geri tepkime hızı azalır.
C) Toplam basınç artar.
D) Denge sabitinin değeri artar.
E) X gazinin mol sayısı azalır.
