Tepkime Hızları Soruları

Kimya
Tepkime Hızları2
eat
= 15.10-4 M/S
NO3(suda) + H₂(g)
2
0125
l koşullar altında H₂ gazının
ğuna göre, Na(k) nin harcan-
5 mol/dak
moldk
/benimhocam
●
4 mol gaz
HCl + H₂O H₂O + Cl¯
TUZAK SORU
T sabit denmezse
Asit ve baz çözeltilerinde
ortamın pH durumuna göre
tepkime hızı belirlenir.
C(k) + O2(g)
-
1 mol 1 mol
CO2(g)
+ISI
vardır.
Hacim
değişir.
Çarpışma Teorisi
Bir tepkime, tepkimeye giren taneciklerin çarpışarak ürün oluş-
turmasıyla gerçekleşir. Tepkimelerin ürün oluşumuyla sonlanan
çarpışmalar etkin çarpışma olarak adlandırılır.
![K+3M-2T
Yukandaki tepkimenin hizi, K'ye göre 2. dereceden
Mye göre 1. derecedendir.
[K] = 0,01 molar, [M] = 0,1 molar alındığında tep-
kime hızı 10 M/s olduğuna göre hız sabiti k'nın
değeri kaçtır?
A) 0,1
B) 1
D) 10
E) 20](https://media.kunduz.com/media/question/seo/raw/20230303134842577319-5002021.jpg?w=256)
Kimya
Tepkime HızlarıK+3M-2T
Yukandaki tepkimenin hizi, K'ye göre 2. dereceden
Mye göre 1. derecedendir.
[K] = 0,01 molar, [M] = 0,1 molar alındığında tep-
kime hızı 10 M/s olduğuna göre hız sabiti k'nın
değeri kaçtır?
A) 0,1
B) 1
D) 10
E) 20
![2X + 3Y Z+2K
tepkimesi için sabit sıcaklıkta deney sonuçları aşağıda-
ki tabloda verilmiştir.
Deney [X] (mol/L)
1
2
3
0,02
0,01
0,03
[Y] (mol/L)
0,02
0,02
0,04
E
Hız (mol/L.s)
2.10-4
1.10-4
1,2.10-3
Buna göre tepkime hız sabitinin sayısal değerini ve
birimini bulunuz.
Ive 2 de y selit
raxt
£ 3
A W
1.102. 2.102](https://media.kunduz.com/media/question/seo/raw/20230303134154208027-4698542.jpg?w=256)
Kimya
Tepkime Hızları2X + 3Y Z+2K
tepkimesi için sabit sıcaklıkta deney sonuçları aşağıda-
ki tabloda verilmiştir.
Deney [X] (mol/L)
1
2
3
0,02
0,01
0,03
[Y] (mol/L)
0,02
0,02
0,04
E
Hız (mol/L.s)
2.10-4
1.10-4
1,2.10-3
Buna göre tepkime hız sabitinin sayısal değerini ve
birimini bulunuz.
Ive 2 de y selit
raxt
£ 3
A W
1.102. 2.102

Kimya
Tepkime Hızları2. Tepkime hız denkleminde derişimlerin üslerinin top-
lamı tepkimenin derecesini verir.
Buna göre, aşağıdaki tek basamaklı tepkimeler-
den hangisinin derecesi yanlıştır?
(2002(g)
D) 2NO
\B))
+102 (9)
Le N₂(g) + 3H₂(g)
(g)
Tepkime
EX HCl(a)
<-> 2CO
(g)
+ O2(g)
CO2(g)
+ O2(g)
2NH3(g)
2NO 2(g)
¹/2H2(g) + ¹/2Cl2(g)
→ 2NO,
Derece
2
R1
4
3
1

Kimya
Tepkime HızlarıNCI
.*.
NE
B/
sin
mle
T
2CO(g) + O₂(g) → 2CO₂(g)
tepkimesinin hızını ölçmek isteyen bir öğrenci;
1. Sabit hacimli kapalı bir kapta, sabit sıcaklıktaki basınç
değişimini takip etme
el
II. Sabit basınçlı bir kapta, sabit sıcaklıktaki hacim değişi-
mini takip etme
III. Elektrik iletkenliğini takip etme
yöntemlerinden hangilerini kullanabilir?
A) Yalnız I
B) Yalnız II
B ve III
E) I, II ve I
Cve Il
20

Kimya
Tepkime HızlarıOP00-11.03KT07
Testokullor
1.
Kapalı bir kapta gerçekleşen
N₂O(g) + NO(g)
N₂(g) + NO₂(g)
tepkimesinde tepkimeye giren moleküllerin çarpışmala-
rının doğrultuları aşağıdaki şekilde modellenmiştir.
1
III
NNO
ONN
BKS
D) I ve II
HEY
ONN
NN
O
NO
NO
Tepkime ürünleri olan N₂ ve NO₂ moleküllerinin model-
leri ise
B) Yalnız II
TEPKİME HIZI
3.
ON
NEY PAL
N DOMS
O
song minsanlegge
şeklinde gösterilebilir.blo a. Jiem to,0
Stueulo obohi
Buna göre reaktiflerin hangi çarpışmaları sonunda
N₂ ve NO₂ ürünlerini vermek üzere tepkime gerçek-
leşebilir?
2
A) Yalnız I
35
E) I ve III
C) Yalnız III

Kimya
Tepkime HızlarıSabit hacim ve sıcaklıkta gerçekleştirilen,
N₂O(g) + ¹/₂O₂(g) → 2NO(g) tepkimesinde,
N₂O gazının harcanma hızı = r₂₁
O₂ gazının harcanma hızı = r₂
NO gazının oluşma hızı = 3
şeklindedir.
Buna göre; r₁ r₂ ve r arasındaki ilişki aşağıda-
2
kilerden hangisinde doğru olarak verilmiştir?
3
A) ²1/12 = 21₂2 = 1/2/2
O
4
B) r₁ = 2r₂ = 4r3
D) 4r₁ = 1/2 = 13
E) r₁ = 2r₂ = 2r3
6
Kimya
Tepkime Hızlarıerji
-ëis
Yayınlan
5.
ev
A) Yalnız
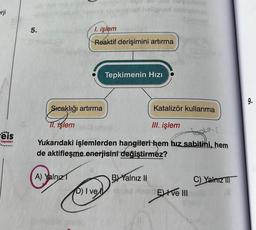
1. işlem
Reaktif derişimini artırma
Sıcaklığı artırma
TI. işlem
hollaned nebralmen
Katalizör kullanma
III. işlem
Yukarıdaki işlemlerden hangileri hem hız sabitini, hem
de aktifleşme enerjisini değiştirmez?
Tepkimenin Hızı
B Yalnız II
D) I vey
Extve III
C) Yalnız
e
6

Kimya
Tepkime Hızları3. Kapalı sabit hacimli bir kapta,
H₂(g) + CO₂(g)
H₂O(s) + CO(g)
tepkimesi tek basamakta gerçekleşmektedir.
Bu tepkimenin hızı,
I. kaba CO₂(g) eklemek,
II. sıcaklığı artırmak,
III. inhibitör kullanmak
işlemlerinden hangileriyle azalır?
A) Yalnız I
b
I ya da II
B) Yalnız II
E) Il ya da III
Yalnız III

Kimya
Tepkime Hızları3.
5,6 gram N₂ gazi;
N₂(g) +20₂(g) → N₂O(g)
denklemine göre yeterince O₂ ile 100 saniyede
tamamen N₂O4 gazına dönüşüyor.
Buna göre bu tepkimede O₂ gazının
harcanma hızı (rO₂) ve N₂O4 hazının oluşum
hızı (rN₂O) NŞA kaç L/s'dir? (N: 14)
r0₂
rN₂04
A 8,96.10-2
B) 2,24.10-3
C) 4,48.10-2
D) 3,36.10-2
E) 8,96.10-3
4,48.10-²
4,48.10-3
2,24.10-²
6,72.10-²
4,48.10-3
ayn
tepl
git

Kimya
Tepkime Hızları2. Şekildeki sistemde bulunan ikinci kapta
A2(g) + 2B2(g)
tepkimesi tek adımda
2mol B2
6L
1
2AB2(g)
A) 9 katına çıkar
C) / üne düşer
gerçekleşmektedir.
K
1mol A2
1mol B2
3L
Aynı tepkime K musluğu açılarak sabit
sıcaklıkta gerçekleştirilirse, tepkime hi-
zı nasıl değişir?
||
B) 3 katına çıkar
D) / s sına düşer
E) - üne düşer
/
MİRAY YAYINLARI
![7. Harcanma ve oluşma hızları arasındaki
ilişki
At
şeklinde olan gaz fazındaki bir tepkime-
nin denklemi aşağıdakilerden hangisi
olabilir?
A) X+3Y
(g)
(g)
B) X(g) + 2Y(g)
C) 2X) + 3Y
(g)
[Y] =+3[Z]
At
At
(g)
2Z
(g)
3Z₁
(g)
2Z
22 (9)
32 (0)
21 (9)
(g)
D) 2X + Y
(g) 1.197
E) 3X(g) + 2Y(g) 2(g)
MÍRAY YAYINLARI](https://media.kunduz.com/media/question/seo/raw/20230303095319405753-3712721.jpg?w=256)
Kimya
Tepkime Hızları7. Harcanma ve oluşma hızları arasındaki
ilişki
At
şeklinde olan gaz fazındaki bir tepkime-
nin denklemi aşağıdakilerden hangisi
olabilir?
A) X+3Y
(g)
(g)
B) X(g) + 2Y(g)
C) 2X) + 3Y
(g)
[Y] =+3[Z]
At
At
(g)
2Z
(g)
3Z₁
(g)
2Z
22 (9)
32 (0)
21 (9)
(g)
D) 2X + Y
(g) 1.197
E) 3X(g) + 2Y(g) 2(g)
MÍRAY YAYINLARI
![12. 2X(g) + 3Y₂(g) → X₂Ye(g)
N₂0
(k) 2.10-1 dir.
C) Aynı sıcaklıkta X, Y ve Z gazlarının derişimleri 2'şer kati-
na çıkanılırsa tepkime hızı 16 katına çıkar.
D) Tepkime mekanizmalı (çok basamakli) gerçekleşir.
E) Aynı sıcaklıkta X, Y, Z gazlarinin derişimleri sırası ile 0,2
mol/L, 0,1 mol/L: 0,4 mol/L alindiğinda T gazının oluşma
hizi 3,2.10-3 mol/L.s'dir.
Rod
11. C
Tepkimesine ait aynı sıcaklıktaki deneysel veriler aşağıdaki
tabloda verilmiştir.
Deney
1
2
3
[X]
(mol/L)
1.10-2
2.10-2
3.10-2
Buna göre,
1. Hız denklem
r = k.[X]. [₂]
III. Yavaş basamak X + Y₂- üründür.
yargılarından hangileri doğrudur?
A) Yalnız!
B) I ve II
12. E
[Y₂]
(mol/L)
1.10-3
3.10-3
4.10-3
şeklindedir.
II. [X]= 1. 10-5 M, Y₂] = 1. 10-4 M alındığında tepkime hızı
1.10€ M/s olur.
D) II ve III
Hız (mol/L.s)
1.10-2
6.10-2
1,2.10-1
C) I ve III
E) I, II ve Ill
175](https://media.kunduz.com/media/question/seo/raw/20230303094334944154-1425661.jpg?w=256)
Kimya
Tepkime Hızları12. 2X(g) + 3Y₂(g) → X₂Ye(g)
N₂0
(k) 2.10-1 dir.
C) Aynı sıcaklıkta X, Y ve Z gazlarının derişimleri 2'şer kati-
na çıkanılırsa tepkime hızı 16 katına çıkar.
D) Tepkime mekanizmalı (çok basamakli) gerçekleşir.
E) Aynı sıcaklıkta X, Y, Z gazlarinin derişimleri sırası ile 0,2
mol/L, 0,1 mol/L: 0,4 mol/L alindiğinda T gazının oluşma
hizi 3,2.10-3 mol/L.s'dir.
Rod
11. C
Tepkimesine ait aynı sıcaklıktaki deneysel veriler aşağıdaki
tabloda verilmiştir.
Deney
1
2
3
[X]
(mol/L)
1.10-2
2.10-2
3.10-2
Buna göre,
1. Hız denklem
r = k.[X]. [₂]
III. Yavaş basamak X + Y₂- üründür.
yargılarından hangileri doğrudur?
A) Yalnız!
B) I ve II
12. E
[Y₂]
(mol/L)
1.10-3
3.10-3
4.10-3
şeklindedir.
II. [X]= 1. 10-5 M, Y₂] = 1. 10-4 M alındığında tepkime hızı
1.10€ M/s olur.
D) II ve III
Hız (mol/L.s)
1.10-2
6.10-2
1,2.10-1
C) I ve III
E) I, II ve Ill
175

Kimya
Tepkime Hızları06
Aşağıda verilen tepkimelerden hangisinin hız
tayininde kullanılan yöntem yanlıştır?
Kazal
A)
B)
C)
D)
E)
N₂O4(9)
(Renksiz)
PCI 5(9)
Tepkime
C(K)
+ O2(g)
Mg(K)
2NO.
CO2(g)
+ H₂O(s)
H(suda) + HCO 3(suda)
2(g)
+ 2HCI,
(Renkli)
PCI 3(g) + Cl2(g)
CO₂
2(g)
(suda)
MgCl2(suda) + H₂(g)
Yöntem
Renk değişimi
Sabit hacim ve
sıcaklıkta basınç
artışı
İletkenlik artışı
Sabit basınç ve
sıcaklıkta hacim
değişimi
pH değişimi
3. Sabit ha
F
yukarıd
yanlışt
A) F
B) H
D)
E)
S
F

Kimya
Tepkime Hızları15.
Bir tepkimenin tepkime derecesini
25
Sıcaklık
Tepkimedeki maddelerin katsayısı
IL Maddenin fiziksel hali
özelliklerinden hangileri belirler?
A+Yalnız II
B) I ve II
byli ve th
C) I ve III
E) I, D ve III

Kimya
Tepkime Hızları1.
212 ONS
3
Al(k)+3KOH(suda) →→ K₂AIO3(suda) +
H₂(g)
2
0, 0śnd
tepkimesine göre 5,4 g Al ile 0,1 M 500 mL KOH çözeltisi
arasındaki reaksiyon 2 dakika sürmektedir.
Buna göre, NK da H₂ gazının oluşma hızı kaç L/dk dır?
(Al:27 g/mol)
(A) 0.28
B) 0,56
C) 1,12 D) 2,24 E) 3,36
4.
