Tepkime Hızları Soruları

Kimya
Tepkime Hızları4
KİMYA
7.
Aynı ortamda eşit derişimli HCI çözeltileri ile
gerçekleştirilen aşağıdaki tepkimelerden hangisi en hızlı
gerçekleşir? (Zn, 26 Fe, 12Mg, 11Na, 19K)
30
-
A) Zn(k) + 2HCl(suda) → ZnCl₂(k) + H₂(g)
B) Fe(k) + 2HCl(suda) → FeCl₂(k) + H₂(g)
C) Mg(k) + 2HCl(suda) →→→ MgCl₂(k) + H₂(g)
D) Na(k) + HCl(suda) → NaCl(k) + 1/2 H₂(g)
E) K(k) + HCl(suda) →KCI(k) + 1/2 H₂(g)

Kimya
Tepkime Hızları1 Sabit sıcaklıkta bir tepkimenin mekanizması şöyledir:
1. F₂ →2F
11. F+CHF3 → HF + CF₂
II. CF, +F→ CF4
Buna göre, aşağıdaki bilgilerden hangisi doğrudur?
(hızlı)
(yavaş)
(hızlı)
Tepkime 3. dereceden gerçekleşir.
BY Katalizör I. basamağa etki eder.
C) Net tepkime F₂ + CHF3 → CF + HF şeklindedir.
D) Tepkimenin ara ürünleri F ve CHF, dür.
CF, maddesi katalizördür.
C

Kimya
Tepkime Hızlarıve
en
0
Sabit sıcaklıkta bir tepkimenin mekanizması şöyledir:
(hızlı)
(yavaş)
(hızlı)
LF₂→2F
IL F+ CHF3 → HF + CF₂
M. CF₂ +F→ CF4
Buna göre, aşağıdaki bilgilerden hangisi doğrudur?
Tepkime 3. dereceden gerçekleşir.
BY Katalizör I. basamağa etki eder.
C) Net tepkime F₂ + CHF3 → CF + HF şeklindedir.
D) Tepkimenin ara ürünleri F ve CHF, dür.
CF, maddesi katalizördür.

Kimya
Tepkime Hızları3
2NH₂ → N₂ + 3H₂
Gaz fazı tepkimesinde NH₂'ün ortalama harcanma hızı 0,01
mol/s dir.
Buna göre, N₂ ve H₂'nin normal koşullarda ortalama oluş-
ma hızı aşağıda hangi seçenekte doğru verilmiştir?
A)
B)
C)
D)
E)
N₂'nin oluşma hızı ( -
S
0,005
1,12
0,112
22,4
2,24
H₂'nin oluşma hızı (
0,015
3,36
0,336
67,8
33,6
![Tek basamakta gerçekleşen,
+ O₂(g) → 2NO2(g)
2NO+0₂
(g)
tepkimesi ile ilgili,
1.
-A[NO] =
2At
11. -A[0₂]
II.
At
III. -A[NO]
At
-A[0,]
At
A) Yalnız I
+A[NO₂]
2At
-A[NO,]
At
hız bağıntılarından hangileri doğrudur?
C
D) II ve III
B) Yalnız II
E) Il ve III
I ve I](https://media.kunduz.com/media/question/seo/raw/20230224200624112612-4803558.jpg?w=256)
Kimya
Tepkime HızlarıTek basamakta gerçekleşen,
+ O₂(g) → 2NO2(g)
2NO+0₂
(g)
tepkimesi ile ilgili,
1.
-A[NO] =
2At
11. -A[0₂]
II.
At
III. -A[NO]
At
-A[0,]
At
A) Yalnız I
+A[NO₂]
2At
-A[NO,]
At
hız bağıntılarından hangileri doğrudur?
C
D) II ve III
B) Yalnız II
E) Il ve III
I ve I

Kimya
Tepkime HızlarıTE 14: TEPKIME
sonuçları
e Hizi
-3
-3
-3
28
için;
Hin louk
→XO. +2AO.
2(g)
XA2(g) + 302 2(g)
Tek basamakta gerçekleşen yukarıdaki
tepkimede hız sabitinin birimi aşağıdaki
lerden hangisidir?
Bilgi: Tepkime hızının birimi mol.L¹.s' dir.
A)
L³
mol ³.s
D)
B)
mol³.s
L³
mol².s
E)
2(g)
C)-
L
mol.s
mol²
L².S
men
1. 2Y
II. T+
III. K
Buna
11.
T
V.F
yar
![24
+0
2(g)
(k)
→ XO2(g)
Sabit hacimli bir kapta tek adımlı gerçek-
leşen yukarıdaki tepkime ile ilgili,
1. Tepkime hızı basınç değişimi ile takip edi-
lebilir.
II. X katı kütlesindeki azalma hızı oksijenin
(O₂) kütlesindeki azalma hızına eşittir.
III. Hız denklemi
Hız = k [0₂]¹ dir.
yargılarından hangileri doğrudur? (C: 12,
0:16)
A) Yalnız I
D) I ve II
B) Yalnız II
C) Yalnız III
E) II ve III
kim
ÇOK V
TEPK
➤ K
A
A
ma
bir
şe
Bi
de
m
le
aA
Te
H
(a
29
CE
➤ H
➤ H](https://media.kunduz.com/media/question/seo/raw/20230224200509551383-4803558.jpg?w=256)
Kimya
Tepkime Hızları24
+0
2(g)
(k)
→ XO2(g)
Sabit hacimli bir kapta tek adımlı gerçek-
leşen yukarıdaki tepkime ile ilgili,
1. Tepkime hızı basınç değişimi ile takip edi-
lebilir.
II. X katı kütlesindeki azalma hızı oksijenin
(O₂) kütlesindeki azalma hızına eşittir.
III. Hız denklemi
Hız = k [0₂]¹ dir.
yargılarından hangileri doğrudur? (C: 12,
0:16)
A) Yalnız I
D) I ve II
B) Yalnız II
C) Yalnız III
E) II ve III
kim
ÇOK V
TEPK
➤ K
A
A
ma
bir
şe
Bi
de
m
le
aA
Te
H
(a
29
CE
➤ H
➤ H

Kimya
Tepkime Hızlarıden hangisi
almasi
et etmesi
as
inin düşmesi
mak için,
mak
PT
te
CA
1. Kap
Hal
2(g)
V=Sbt
T=Sbt
Ideal piston
Yukarıdaki kaplarda belirtilen şartlarda,
→ 2HCl (g)
Halal + Cl2(g)
2(g)
Tepkimesi eşit hızlarda gerçekleşirken her
iki kabada aynı sıcaklıkta He gazı gönderi-
lirse tepkime hızları nasıl etkilenir?
Artar
B) Azalır
C) Artar
D) Değişmez
E) Değişmez
H₂i)
Cl₂
P = Sbt
T=Sbt
II. Kap
Artar
Azalır
Azalır
Azalır
Değişmez
Kimya
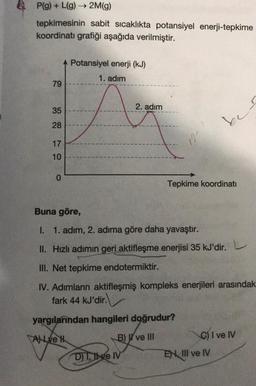
Tepkime HızlarıP(g)+L(g) → 2M(g)
tepkimesinin sabit sıcaklıkta potansiyel enerji-tepkime
koordinati grafiği aşağıda verilmiştir.
79
35
28
17
10
0
A Potansiyel enerji (kJ)
1. adım
2. adım
DIT, ve IV
1.27
yargılarından hangileri doğrudur?
Ave H
B) ve III
Tepkime koordinati
Buna göre,
I. 1. adım, 2. adıma göre daha yavaştır.
II. Hızlı adımın geri aktifleşme enerjisi 35 kJ'dir.
III. Net tepkime endotermiktir.
IV. Adımların aktifleşmiş kompleks enerjileri arasındak
fark 44 kJ'dir.
bes
C) I ve IV
EX, Ill ve IV
![. TEST
3.
5. Unite / KIMYASAL TEPKİMELERDE HIZ
A(g) + 2B(g) + C(g)
<-3D(g)
tepkimesi için belirli bir sıcaklıkta yapılan deneylerden aşağı-
daki veriler elde edilmiştir.
De-
ney
1
2
3
4
[A]
(mol/L)
0,1
0,1
0,2
0,2
D) k.[A].[C]
E) k. [A]².[C]
A) k.[A].[B]².[C]
B) k.[A].[C]2
C) k.[C]²
[B]
[C]
(mol/L) (mol/L)
0,2
0,4
0,4
3.10-3
3.10-3
12.10-3
0,1
24.10-3
Buna göre, tepkimenin hız bağıntısı aşağıdakilerden
hangisidir?
0,2
0,2
0,2
0,4
Hız
(mol/L.s)](https://media.kunduz.com/media/question/seo/raw/20230224184951771494-5201948.jpg?w=256)
Kimya
Tepkime Hızları. TEST
3.
5. Unite / KIMYASAL TEPKİMELERDE HIZ
A(g) + 2B(g) + C(g)
<-3D(g)
tepkimesi için belirli bir sıcaklıkta yapılan deneylerden aşağı-
daki veriler elde edilmiştir.
De-
ney
1
2
3
4
[A]
(mol/L)
0,1
0,1
0,2
0,2
D) k.[A].[C]
E) k. [A]².[C]
A) k.[A].[B]².[C]
B) k.[A].[C]2
C) k.[C]²
[B]
[C]
(mol/L) (mol/L)
0,2
0,4
0,4
3.10-3
3.10-3
12.10-3
0,1
24.10-3
Buna göre, tepkimenin hız bağıntısı aşağıdakilerden
hangisidir?
0,2
0,2
0,2
0,4
Hız
(mol/L.s)

Kimya
Tepkime Hızlarıfer
a-
20. X2(g) + 3Y2(g) 2XY,
3(g)
tepkimesine ait potansiyel enerji (P-E) tepkime koordina
ti grafiği aşağıdaki gibidir.
Potansiyel enerji (ki)
36
14.8
65
F1 / DENEME-9 A
TA
30
X2(g) +3Y2(g)
5
2XY3
Y 3(g)
Tepkime koordinati
Grafiğe göre tepkime ile ilgili aşağıdaki ifadelerden
hangisi yanlıştır?
65
A) Aktifleşmiş kompleksin enerjisi 35 kj'dir.
B) Ürünlerin potansiyel enerjileri toplamı 5 kj'dir.
L
C) Tepkime entalpisi -25 kj'dir.
L
D) 2XY 3(g) → X2(g) +3Y2(g) tepkimesinin aktifleşme
enerjisi 60 kj'dir.
E) Tepkime ekzotermiktir.

Kimya
Tepkime Hızları2.
P.E
A
A) 4 katına çıkar.
C) 12 katına çıkar.
T.K
Mekanizması
1. adım XY₂(g) + 2Z₂(g) →→→XY₂Z(g) + 3Z(g)
II. adım XY₂(g) + Z(g) →→→→XY₂Z(g)
şeklinde olan tepkimenin potansiyel enerji (P.E)-tepkime
koordinatı (T.K) grafiği yukarıda verilmiştir.
Bu bilgilere göre, Z, gazının başlangıç derişimi 2 ka-
tina, XY₂ gazının başlangıç derişimi 3 katına çıkarılırsa
tepkime hızı nasıl değişir?
2
E) 64 katına çıkar.
B) 8 katına çıkar.
D) 16 katına çıkar.
Palme Yayınevi
20100+ 3H.SQ.(syda) →→→ Al₂(SO) (suda) + 3H₂(g)
Kimya
Tepkime Hızları4 20.
1
3
Potansiyel Enerji (kj)
190
a
b
I. adım
II. adım
436-3
1
est
393
11
634
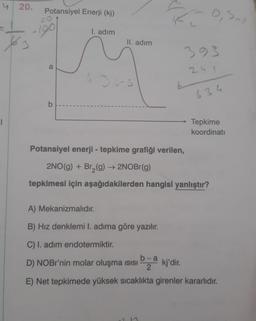
Potansiyel enerji - tepkime grafiği verilen,
2NO(g) + Br₂(g) → 2NOBr(g)
tepkimesi için aşağıdakilerden hangisi yanlıştır?
Tepkime
koordinati
A) Mekanizmalıdır.
B) Hız denklemi I. adıma göre yazılır.
C) I. adım endotermiktir.
D) NOBr'nin molar oluşma ısısı
bakj'dir.
E) Net tepkimede yüksek sıcaklıkta girenler kararlıdır.
![42.
→→→
aX(g) + bY(g) →→→ cZ(g)
cZ(g)Onsion
tepkimesi için sabit sıcaklıkta yapılan deneyler ve sonuç-
ları tabloda verilmiştir.
Deney
no
1
2
[X]
(mol/L)
0,1
0,2
A) r=k.[X]2.[Y]
C) r=k. [X].[Y]²
[Y]
(mol/L)
0,4
0,1
Başlangıç hızı
(mol/L.s)
r₁
Bu deneylerde ölçülen tepkimelerin hızları eşit (r₁=r₂)
olduğuna göre tepkimenin hız bağıntısı aşağıdakiler-
den hangisi olabilir?
E) r=k. [X]. [Y]³
r₂
B) r=k. [X].[Y]
D) r=k.[X]²](https://media.kunduz.com/media/question/seo/raw/20230224180034378822-4930127.jpg?w=256)
Kimya
Tepkime Hızları42.
→→→
aX(g) + bY(g) →→→ cZ(g)
cZ(g)Onsion
tepkimesi için sabit sıcaklıkta yapılan deneyler ve sonuç-
ları tabloda verilmiştir.
Deney
no
1
2
[X]
(mol/L)
0,1
0,2
A) r=k.[X]2.[Y]
C) r=k. [X].[Y]²
[Y]
(mol/L)
0,4
0,1
Başlangıç hızı
(mol/L.s)
r₁
Bu deneylerde ölçülen tepkimelerin hızları eşit (r₁=r₂)
olduğuna göre tepkimenin hız bağıntısı aşağıdakiler-
den hangisi olabilir?
E) r=k. [X]. [Y]³
r₂
B) r=k. [X].[Y]
D) r=k.[X]²

Kimya
Tepkime Hızları16. Gaz fazında gerçekleşen bir tepkimeye ait molekül sayı-
si-kinetik enerji dağılımı grafiği aşağıda verilmiştir.
Molekül sayısı
Eşik enerjisi
D)
T₁
T₂
Buna göre,
T₁, sıcaklığında tepkime hızı daha fazladır.
II. T₂ sıcaklığında ortalama kinetik enerji daha fazladır.
NYX.
T, sıcaklığı, T₂ sıcaklığından daha düşüktür.
yargılarından hangileri doğrudur?
A) Yalnız
BYalnız II
Kinetik enerji
C) Yalnız III
E) I ve III

Kimya
Tepkime Hızları3.
2H₂O₂(suda)
2H₂O(s) + O₂(g)
denklemine göre gerçekleşen tepkimede H₂O₂ derişiminin,
200. saniyede 2,00 mol/L
• 600. saniyede 1,40 mol/L
olduğu tespit ediliyor.
Buna göre, verilen zaman aralığında H₂O, nin ortalama bo-
zunma hızı kaç mol/L.s dir?
A) 1,8x10-2
300 sn → 0,6l/L
5005 mol/L
D) 1,5x10-3
B) 1,5x10-2
E) 1,0x10-3
C) 1,0x10-2
