Tepkime Hızları Soruları
Kimya
Tepkime Hızları3.
90
50
20
ğuna göre x
hangisidir?
A) 67 B) 63
1
C) 60
2
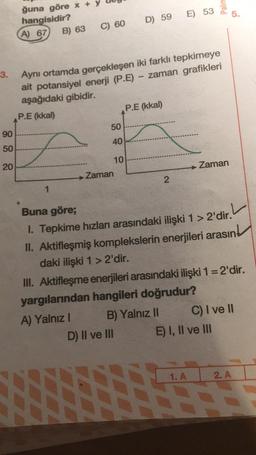
Aynı ortamda gerçekleşen iki farklı tepkimeye
ait potansiyel enerji (P.E) - zaman grafikleri
aşağıdaki gibidir.
P.E (kkal)
50
40
→→ Zaman
D) 59 E) 53
10
P.E (kkal)
D) II ve III
2
B) Yalnız II
Palm
Buna göre;
1. Tepkime hızları arasındaki ilişki 1 > 2'dir.
II. Aktifleşmiş komplekslerin enerjileri arasın
daki ilişki 1 > 2'dir.
Zaman
III. Aktifleşme enerjileri arasındaki ilişki 1 = 2'dir.
yargılarından hangileri doğrudur?
A) Yalnız I
1. A
5.
E) I, II ve III
C) I ve II
2. A

Kimya
Tepkime Hızları11.
12
D) I ve III
E) I, II ve III
N₂(g) +202(g)
-
2NO2(g)
Tepkimeşi 2 litrelik bir kapta sabit sıcaklıkta gerçekleşmek-
tedir.
oth
→
N₂(g) + 3H₂(g) -
N2 gazının mol sayısı 10 saniyede 0,8 mol'den 0,4 mole
düştüğüne göre NO2 gazının bu zaman aralığında or-
talama oluşma hızı kaç mol/L.s'dir?
A) 0,01
B) 0,02 C) 0,04
D) 0,08
E) 0,2
0122015
→ 2NH3(g)
01
![2. Gaz fazında tam verimle artansız gerçekleşen bir tepkime-
de girenler ve ürünler arasındaki hız ilişkisi,
-A[A]
3 At
şeklindedir.
Buna göre tepkimeyle ve tepkimede yer alan madde-
lerle ilgili aşağıdakilerden hangisi yanlıştır?
A) Tepkime denklemi,
r =
-A[B]
At
=
=
+A [C]
2 At
=
+A[D]
2 At
3A(g) + B(g) 2C(g) + 2D(g) şeklindedir.
B) Tepkime hızı en büyük olan A'dır.
C) C ve D'nin oluşma hızları eşittir.
D) A'nın tükenmesi için geçen süre B'nin tükenmesi için
geçen sürenin 3 katıdır.
E) B'nin harcanma hızı C'nin oluşma hızının yarısı kadardır.
Orbital Yayınları](https://media.kunduz.com/media/question/seo/raw/20230318180116063152-956761.jpeg?w=256)
Kimya
Tepkime Hızları2. Gaz fazında tam verimle artansız gerçekleşen bir tepkime-
de girenler ve ürünler arasındaki hız ilişkisi,
-A[A]
3 At
şeklindedir.
Buna göre tepkimeyle ve tepkimede yer alan madde-
lerle ilgili aşağıdakilerden hangisi yanlıştır?
A) Tepkime denklemi,
r =
-A[B]
At
=
=
+A [C]
2 At
=
+A[D]
2 At
3A(g) + B(g) 2C(g) + 2D(g) şeklindedir.
B) Tepkime hızı en büyük olan A'dır.
C) C ve D'nin oluşma hızları eşittir.
D) A'nın tükenmesi için geçen süre B'nin tükenmesi için
geçen sürenin 3 katıdır.
E) B'nin harcanma hızı C'nin oluşma hızının yarısı kadardır.
Orbital Yayınları
Kimya
Tepkime Hızları7.
1,5-
1,0
0,5
10
20
30
Zaman (s)
Orbital Yayınları
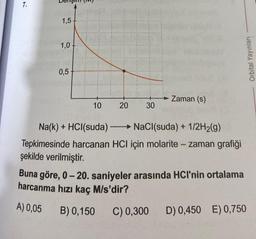
Na(k) + HCl(suda)
NaCl(suda) + 1/2H₂(g)
Tepkimesinde harcanan HCI için molarite - zaman grafiği
şekilde verilmiştir.
Buna göre, 0 -20. saniyeler arasında HCI'nin ortalama
harcanma hızı kaç M/s'dir?
A) 0,05 B) 0,150 C) 0,300 D) 0,450 E) 0,750

Kimya
Tepkime HızlarıTEST 2 KIMYASAL TEPKİMELERDE HIZ
la-
|
Orbital Yayınları
4.
COCI2(g)
CO(g) + Cl₂(g)
0,6 mol COCl2 gazı sabit sıcaklıkta 2 litrelik bir kapta 30
saniyede tamamen parçalanıyor.
Buna göre COCI2 gazının ortalama harcanma hızı kaç
mol/L.s'dir?
A) 0,6
B) 0,3
C) 0,06 D) 0,03
E) 0,01

Kimya
Tepkime Hızları5.
X
2
+2SO2(g)
+302(g)
CO
219,
CS 21:
tepkimesi sabit sıcaklıkta 40 saniyede gerçekleş-
mektedir.
Bu tepkimede oluşan CO₂ ve SO₂ gazlarının nor-
mal koşullardaki toplam hacmi 13,44 L olduğu-
na göre tepkimenin gerçekleştiği koşullarda CS₂
gazının ortalama harcanma hızı kaç gram/s'dir?
(C: 12, S: 32)
A) 3,8
D) 0,38
B) 1,9
E) 0,19
C) 0,76

Kimya
Tepkime Hızlarımiktar C6H12O6
Iti hazırlanıyor.
daki ifadelerden
ya göre daha
göre daha
ce sıcaklığı
Dört
esl
38
Worth
15. Birim zamanda, ortamda bulunan enzimlerin değiştirdi
substrat molekülü sayısına reaksiyon değişim sayısı d
Buna göre, reaksiyon değişim sayısı;
SAYISI:
I.
substrat yüzeyinin genişliği,
II. aktivasyon enerjisinin miktarı, X
III. ortamın pH değeri,
IV. ortamın sıcaklığı
faktörlerinden hangilerine bağlı olarak değişkenlik
gösterebilir?
A) I ve II
UcDört
Bec
I, III ve IV
B) II ve III
C) III ve
EI, II, III ve IV

Kimya
Tepkime Hızları(s)
an grafi-
i yanlış
2 bulun
H₂(g) + Cl₂(g) → 2HCl(a)
denklemine göre gerçekleşen tepkimede 2 litre ha-
cimli kapta H₂ gazının mol sayısı 200 saniyede 0,9
molden 0,5 mole düşüyor.
Buna göre;
1. H₂ gazının ortalama harcanma hızı 2.10-3 mol/s
dir.
II. HCI gazının ortalama oluşma hızı 2.10-³ mol.L¹-.s¹-
dir.
III. Tepkime homojendir.
ifadelerinden hangileri doğrudur?
B) I ve II
A) Yalnız I
D) II ve III
E) I, II ve III
4.
C) I ve III

Kimya
Tepkime Hızları8.
N2(g)
+ 3H2(g)
3
3
3 er mol N₂ ve H₂ gazlarının 500 mililitre hacimli kap-
taki tam verimli tepkimesi 400 saniyede tamamlanı-
yor.
Buna göre;
→ 2NH3(g)
I. NH₂'ün oluşma hızı 1.10-2 mol.L-1.s-¹ dir.
II. Saniyede ortalama 1,5.10-2 gram H₂ harcanır.
III. N₂'nin ortalama bozunma hızı 5.10-3 mol.L-1.s-1
dir.
ifadelerinden hangileri doğrudur? (H = 1, N = 14)
B) I ve II
A) Yalnız I
D) II ve III
E) I, II ve III
C) I ve III

Kimya
Tepkime Hızlarıme-
nti-
21. PCI, gazi,
PCI (g) → PCI(g) + Cl₂(g)
denklemine göre, PCI, ve Cl₂ gazlarına dönüş-
mektedir.
PCI moleküllerinin iki farklı sıcaklıktaki kinetik
enerji dağılımı aşağıdaki grafikte verilmiştir.
Molekül sayısı
T₂ ST₁
√₂)(a
Ea
Snus
L
12
Buna göre,
1. T₂ > T₁ dir.
II. T, sıcaklığındaki tepkimenin aktifleşme enerjisi
1
daha büyüktür.
D) I ve III
Kinetik enerji
III. T₂ sıcaklığındaki tepkimenin hızı daha büyük-
tür.
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız II
C) Yalnız III
E) I, II ve III
ay (0
Konu Tarama Testi | Kimya
![i de-
abi-
1. Sabit sıcaklıkta kapalı kapta gerçekleşen;
3X(g) + 2Y(g) + Z(g) → ürünler
tepkimesine ait başlangıç derişimlerini ve başlangıç hızla-
rını gösteren deney sonuçları tablodaki gibidir.
[X]M [Y]M [Z]M
Hız (mol/Ls)
0,1
0,3
0,1
2-10-3
0,1
0,6
0,2
4-10-3
0,1
0,6
0,1
2-10-3
0,3
1,2
0,2
1,2-10-2
Buna göre, aşağıdaki ifadelerden hangisi yanlıştır?
Deney
1
23
4
A) Tepkime hız ifadesi r = K[X][Z] tür.
B) Tepkime tek basamakta gerçekleşmiştir.
C) k, hız sabitinin sayısal değeri 0,2'dir.
L 1
D) K'nın birimi
mol s
E) Y, hız ifadesinde yer almaz.
dir.
for
y
610₂
CN](https://media.kunduz.com/media/question/seo/raw/20230318161734549396-5449297.jpg?w=256)
Kimya
Tepkime Hızlarıi de-
abi-
1. Sabit sıcaklıkta kapalı kapta gerçekleşen;
3X(g) + 2Y(g) + Z(g) → ürünler
tepkimesine ait başlangıç derişimlerini ve başlangıç hızla-
rını gösteren deney sonuçları tablodaki gibidir.
[X]M [Y]M [Z]M
Hız (mol/Ls)
0,1
0,3
0,1
2-10-3
0,1
0,6
0,2
4-10-3
0,1
0,6
0,1
2-10-3
0,3
1,2
0,2
1,2-10-2
Buna göre, aşağıdaki ifadelerden hangisi yanlıştır?
Deney
1
23
4
A) Tepkime hız ifadesi r = K[X][Z] tür.
B) Tepkime tek basamakta gerçekleşmiştir.
C) k, hız sabitinin sayısal değeri 0,2'dir.
L 1
D) K'nın birimi
mol s
E) Y, hız ifadesinde yer almaz.
dir.
for
y
610₂
CN

Kimya
Tepkime Hızları18
1. Her iki çözeltinin de aynı dış basınçta kaynamaya
başlama sıcaklıkları eşittir.
tuzunun 40 °C'deki çözünürlüğü 25 g X/100 g su
11. tuz
II.
dur
H. İlk durumdaki çözeltide bir miktar daha X katısı çö-
zülebilir.
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız II
D) I ve II
2003 0,0015
2X₂Y(g) → 2X₂(g) + Y₂(g)
Eve III
B) 5.10-5
tepkimesi başladıktan 5 dakika sonra X₂Y derişimi
0,003 mol L-1 azalmıştır.
C) Yanız III
Buna göre Y₂ gazının ortalama oluşma hızı kaç mol
L-1 s-1 dir?
A) 5.10-6
D) 6.10-4
5.60 -7 300 Sny
15.10
X₂Y hızı = 0,003
300
500.20
100
E) 3.10-4
C) 1.10-5
310-3
105
(1
35
is
82
20.
![4. Tek adımda X₂ ve Y₂ gazları arasında sabit sıcaklıkta 1
litrelik sabit hacimli kapta gerçekleşen deneylerin sonuçlanı
aşağıda verilmiştir.
[X₂]
(mol/L)
[Y₂]
(mol/L)
0,01
0,03
0,03
Deney
1
2
3
Buna göre,
a) Tepkimenin hız denklemini yazınız.
b) Hız sabitinin sayısal değeri kaçtır?
Başlangıç hızı
(mol/L.s)
0,01
0,01
0,05
1,0x10-6
3,0x10-6
1,5x10-5
c) Tepkimenin mertebesi kaçtır?
d) [X₂] = 0,1 M, [Y₂] = 0,5 M olsaydı tepkime hızının
mol
başlangıç değeri kaç
olurdu?
L.s
2. Ka
t](https://media.kunduz.com/media/question/seo/raw/20230318163137525141-771939.jpg?w=256)
Kimya
Tepkime Hızları4. Tek adımda X₂ ve Y₂ gazları arasında sabit sıcaklıkta 1
litrelik sabit hacimli kapta gerçekleşen deneylerin sonuçlanı
aşağıda verilmiştir.
[X₂]
(mol/L)
[Y₂]
(mol/L)
0,01
0,03
0,03
Deney
1
2
3
Buna göre,
a) Tepkimenin hız denklemini yazınız.
b) Hız sabitinin sayısal değeri kaçtır?
Başlangıç hızı
(mol/L.s)
0,01
0,01
0,05
1,0x10-6
3,0x10-6
1,5x10-5
c) Tepkimenin mertebesi kaçtır?
d) [X₂] = 0,1 M, [Y₂] = 0,5 M olsaydı tepkime hızının
mol
başlangıç değeri kaç
olurdu?
L.s
2. Ka
t

Kimya
Tepkime Hızları1. 2X+Y+Z→ 2D + E
gaz fazında gerçekleşen tepkimesi için sabit sıcaklıkta
başlangıç derişimleri ve tepkime hızı ile ilgili aşağıdaki
veriler elde ediliyor:
- Girenlerin derişimleri 2 şer katına çıkarılınca hız 8 katına
çıkıyor.
X ve Y derişimi sabitken, Z derişimi 3 katına çıkarılınca
hız 9 katına çıkıyor.
Y derişimi sabitken, X ve Z derişimleri 2 şer katına
çıkarılınca hız 8 katına çıkıyor.
Buna göre, tepkimenin hız bağıntısı
...........dir.
![2.
X(g) + Y(g) + 2Z(g) → K(g) + M(g)
tepkimesi ile ilgili olarak sabit sıcaklıkta yapılan deneylerin
sonuçları aşağıda verilmiştir.
[X]
Deney (mol/L)
1
2
3
4
0,01
0,01
0,02
0,03
[Y]
(mol/L)
0,01
0,01
0,01
0,02
[Z]
(mol/L)
Hız
(mol/L.s)
0,02 2x10-4
0,04
8x10-4
0,02 2x10-4
0,01 1x10-4
a) Tepkimenin hız denklemini yazınız.
b) Hız sabitinin deney sıcaklığındaki değerini ve hız
sabitinin birimini bulunuz.
c) Tepkime hızının X, Y ve Z ye göre derecelerini
ve tepkime hızının kaçıncı dereceden olduğunu
bulunuz.
d) [X]=0,1 M, [Y] = 0,2 M, [Z]=0,4 M olsaydı, tepkime
hızı ne olurdu?
e) Tepkime mekanizmalı mıdır? Eğer mekaniz-malıysa
yavaş adımda girenler hangileridir?](https://media.kunduz.com/media/question/seo/raw/20230318163047287060-771939.jpg?w=256)
Kimya
Tepkime Hızları2.
X(g) + Y(g) + 2Z(g) → K(g) + M(g)
tepkimesi ile ilgili olarak sabit sıcaklıkta yapılan deneylerin
sonuçları aşağıda verilmiştir.
[X]
Deney (mol/L)
1
2
3
4
0,01
0,01
0,02
0,03
[Y]
(mol/L)
0,01
0,01
0,01
0,02
[Z]
(mol/L)
Hız
(mol/L.s)
0,02 2x10-4
0,04
8x10-4
0,02 2x10-4
0,01 1x10-4
a) Tepkimenin hız denklemini yazınız.
b) Hız sabitinin deney sıcaklığındaki değerini ve hız
sabitinin birimini bulunuz.
c) Tepkime hızının X, Y ve Z ye göre derecelerini
ve tepkime hızının kaçıncı dereceden olduğunu
bulunuz.
d) [X]=0,1 M, [Y] = 0,2 M, [Z]=0,4 M olsaydı, tepkime
hızı ne olurdu?
e) Tepkime mekanizmalı mıdır? Eğer mekaniz-malıysa
yavaş adımda girenler hangileridir?
![20. 1. adim: X(g) +Y(g)
2. adım: X(g) +Z(g)
Z(g) + T(g)
K(g)
Mekanizması yukarıda verilen tepkime ile ilgili ola-
rak aşağıdaki yargılardan hangisi yanlıştır?
(K= Derişimlere bağlı denge sabiti,
Kp = Kısmi basınçlara bağlı denge sabiti)
A) Z(g) ara üründür.
BY Toplu tepkime denklemi;
2X(g) +Y(g) →→ T(g) + K(g)
şeklindedir.
C) Denge bağıntısı, K =
(Yavaş)
(Hızlı)
[T][K] dır.
[Y].[XR
D) Hız bağıntısı Hız = K.[X].[Y] dır.
E) KK dir.](https://media.kunduz.com/media/question/seo/raw/20230318150716716739-5449297.jpg?w=256)
Kimya
Tepkime Hızları20. 1. adim: X(g) +Y(g)
2. adım: X(g) +Z(g)
Z(g) + T(g)
K(g)
Mekanizması yukarıda verilen tepkime ile ilgili ola-
rak aşağıdaki yargılardan hangisi yanlıştır?
(K= Derişimlere bağlı denge sabiti,
Kp = Kısmi basınçlara bağlı denge sabiti)
A) Z(g) ara üründür.
BY Toplu tepkime denklemi;
2X(g) +Y(g) →→ T(g) + K(g)
şeklindedir.
C) Denge bağıntısı, K =
(Yavaş)
(Hızlı)
[T][K] dır.
[Y].[XR
D) Hız bağıntısı Hız = K.[X].[Y] dır.
E) KK dir.
