Zayıf Etkileşimler Soruları

Kimya
Zayıf Etkileşimler5.
Moleküler Kati
Tanecikleri Bir
Arada Tutan En Etkin
Kuvvetler
1.
Kuru buz (CO2(k) Dipol-dipol etkileşimleri
II.
Kükürt (S8(K)
London etkileşimleri
III. Şeker (C6H12O6K) Hidrojen bağları
Yukarıdaki tabloda bazı moleküler katı örnekleri-
nin taneciklerini bir arada tutan etkin kuvvetler ve-
rilmiştir.
Buna göre hangilerinde yanlışlık yapılmıştır?
A) Yalnız
B) Yalnız III
C) I ve II
D) II ve III
E) I ve III

Kimya
Zayıf Etkileşimler5. Yoğun fazda moleküller arasında London kuvvetleri,
dipol-dipol etkileşimleri, dipol-indüklenmiş dipol etki-
leşimleri ve hidrojen bağlan oluşabilir.
Buna göre, aşağıda verilen moleküller arasında
yoğun fazda oluşabilecek zayif etkileşimlerden
hangisinde baskın etkileşim türü karşısında yanlış
verilmiştir? (H. He, 6.30.15P. 17CI)
Moleküller Baskin etkileşim türü
A) 0₂-0₂ London kuvvetleri
B) H2O-H2O Dipol-dipol etkileşimi
C) He-He
London kuvvetleri
D) PH3 - PH Dipol-dipol etkileşimi
E) HCI-CH4 Dipol-indüklenmiş dipol etkileşimi

Kimya
Zayıf EtkileşimlerCelik kap
Hois)
Çelik bir kapta si halde bulunan H2O molekülleri ve
atomlan arasındaki etkileşim yukanda verilmiştir.
er
a etkileşim: 496 kJ/mol
betkileşim: 43 kJ/mol
Buna göre,
1. H2O SIVISI isitilarak gaz fazına geçirilirse a ve b etki-
leşimleri kopar.
Çelik kaba 550 kJ/mol isi verilirse H2O nun kimyasal
özelliği değişebilir.
III. H2O SIVISi isitilir ve gaz fazına geçirilirse moleküller
arasmdaki hidrojen bağı kopar.
W. a ile gösterilen etkileşim apolar kovalent bağdır.
(voll
ile gösterilen etkileşim zayıf etkileşimdir.
ifadelerinden kaç tanesi doğru verilmiştir?
ES
A) 1
B) 2
C) 3

Kimya
Zayıf Etkileşimlernden
C) Yalnizli
III. I işininin işık şid
işlemlerinden hangileri tek başına yapılabilir?
A) Yalnız!
B) Yalnız II
ninkine
E) II ve III
D) I ve II
en büyüktür.
r?
2S'dir.)
CI ve Il
S S
KÖŞEBILGI Yayınları
S
8.
der.
Elmiştir.
X in yoğun fazlarında moleküller arasında hidrojen
bağı vardır.
-
Y-X karışımında iyon - dipol etkileşimleri etkindir.
Z-X karışımında dipol-dipol etkileşimleri etkindir.
Saf X, Y ve Z maddeleri ile ilgili yukarıda verilen
bilgilere göre, bu maddeler aşağıdakilerden
hangisindeki gibi olabilir?
(H, 6C, 7N, 20, 11 Na, 169, 17C1, 19K, 35Br)
8
X
Y
Z
gisi
A)
KBr
CHCI
H2O
NH
NaCl
CH4
C)
KBY
NHz
D)
HS
HO
@
HO
NH3
CH OH
E)
NaCl
HO
28
Viğe
geçiniz.

Kimya
Zayıf EtkileşimlerAşağıdaki maddeleri yoğun fazda bir arada tutai
etkin etkileşimlerden hangisi doğru verilmiştir?
Maddeler
A)
Cao - HO
B) . CHỊCI - CH CI
Etkin Etkileşim
dipol - dipol
indüklenmiş dipoi -
indüklenmiş dipol
hidrojen baği
dipol - indüklenmiş dipol
dipol-dipol
C)
D
H₂-0₂
1-H₂O
NH, - HF
-
E)
-

Kimya
Zayıf EtkileşimlerAysun, bazı katıların sat su ile etkileşimini incelemek
üzere aşağıdaki deneyleri yapmıştır.
Nal(K)
C6H12O6(K)
CaO)
25°C
25°C
25°C
Saf su
Saf su
Saf su
1
II
III
Buna göre I, II ve III numaralı kaplarda gerçekleşen
olaylar ve çözeltiler ile ilgili olarak Aysun bir rapor
hazırlarsa raporunda yazacağı aşağıdaki
yargılardan hangisi yanlış olur?
A) I. ve II. kapta fiziksel değişme, III. kapta ise
kimyasal değişme olmuştur.
BH. kapta iyon - dipol etkileşimi gerçekleşir.
C. I. ve III. kaptaki çözeltiler elektrolit, II. kaptaki çözelti
ise elektrolit değildir.
D) II. kapta indüklenmiş dipol - dipol etkileşiminin
etkin olduğu motekiler çözünme gerçekleşir.
E) Her üç çözeltinin kaynama noktası aynı koşullarda
sat sudan yüksektir

Kimya
Zayıf EtkileşimlerMadde
Viskozite (Pa.s)
7.
-ene bo
1,0 x 10-3
HH (su)
H H H
1 1
H-C-C-C-H
LI
OH OH OH
1,42
(Gliserin)
Açık yapıları ve 20°C'taki viskozite değerleri
tabloda verilen maddelerden, gliserinin visko-
zitesinin suyunkinden daha yüksek olmasının
nedeni;
1. Gliserinin molekülleri arasında oluşturabile-
ceği hidrojen bağı sayısının, suyunkinden
fazla olması
II. Gliserinin molekülündeki kovalent bağ sayısı-
nin, suyunkinden fazla olması
III. Gliserin molekülleri arasındaki London kuv-
vetlerinin, suyunkinden fazla olması
durumlarından hangileri ile açıklanabilir?
A) Yalnız! B) Yalnız II C) I ve II
D) I ve III E) II ve III

Kimya
Zayıf Etkileşimler12..
B.
Polar çözücüler, polar ve iyonik bağlı maddeleri çö-
zerken; apolar çözücüler
, apolar maddeleri daha iyi
çözer.
Birbiriyle hidrojen bağı oluşturabilen maddelerde
çözünme daha iyi olur.
Buna göre,
Çözücü
Çözünen
1.
HS
e
Caci
HF Pu
II.
HO
WW.
CHOA
CH,20 P
tablodaki maddelerden hangilerinin birbiri içerisinde
çözünmesi beklenir?
GH, 6C, 80, 9F 169, 170, 20Ca)
773762
A) Yalnız II
Byl ve II
C) I ve III
D) II ve III
(E, Il ve III

Kimya
Zayıf Etkileşimler9.
)
CaCO3(k) → COM + CO2(g)
Tepkimesi ile ilgili;
I. Analiz tepkimesidir.
II. Heterojen bir tepkimedir.
III. Oluşan CO2 gazı yanma tepkimesi vermez.
yargılarından hangileri doğrudur?
.
A) Yalnız! B) Yalnız 11 C) Yalnız III
dolata
D) II ve III
E), II ve III
narodowe biels
Hotele
Cimabubb
no sinoda

Kimya
Zayıf EtkileşimlerSoru 12
Madde
Kaynama noktası (°C)
-253
H₂
-196
N2
-183
O2
Bazı moleküllere ait kaynama sıcaklıkları yukarı-
daki gibidir.
O2 molekülünün kaynama noktasının H2 ve N2
moleküllerine göre daha yüksek olması, O2 mo-
lekülünün;
1. Apolar molekül olması
II. Daha fazla elektron içermesi
III. Kalıcı dipol görülmesi
özelliklerinden hangileri ile açıklanabilir?
A) Yalnız
B) Yalnız 11
C) I ve II
D) I ve III
E) II ve III

Kimya
Zayıf Etkileşimler10. Aşağıda verilen madde çiftlerinden hangisi karşısın-
da belirtilen zayıf etkileşim türünü içermez?
Madde çifti
Zayıf etkileşim türü
London etkileşimi
Dipol - indüklenmiş dipol
A) Hz - N2
B) H2O- CO2
C) Mg2+ - H29
D) NH3 - H2
E) CH4 - C2H6
İyon - dipol
Hidrojen bağı
London etkileşimi
-
Kimya
Zayıf EtkileşimlerYeni Nesil Sorular
5.
şim görülebilir
an) etkileşim bir
100. HO
HE
H.To
0-
NH
H. Se
*SbH
- Ash
1
*HI
InHg
WS
HCL
PH
SiH
HBE
100-
şimler,
etkileşim
inde etkileşim
Gel
1
1
20 35 go 130
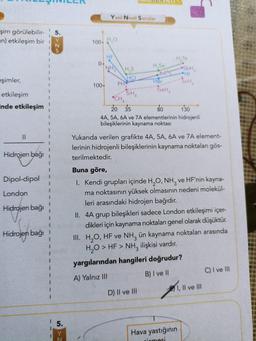
4A, 5A, 6A ve 7A elementlerinin hidrojenli
bileşiklerinin kaynama noktası
II
Hidrojen bağı i
Dipol-dipol
London
Hidrojen bağı
Yukarıda verilen grafikte 4A, 5A, 6A ve 7A element-
lerinin hidrojenli bileşiklerinin kaynama noktaları gös-
terilmektedir.
Buna göre,
1. Kendi grupları içinde H2O, NH3 ve HF'nin kayna-
ma noktasının yüksek olmasının nedeni molekül-
leri arasındaki hidrojen bağıdır.
II. 4A grup bileşikleri sadece London etkileşimi içer-
dikleri için kaynama noktaları genel olarak düşüktür.
III. H2O, HF ve NH, ün kaynama noktaları arasında
H2O > HF > NH, ilişkisi vardır.
yargılarından hangileri doğrudur?
A) Yalnız III
B) I ve 1
C) I ve III
D) II ve III
1. Il ve III
Hidrojen bağı
5.
Y
N
Hava yastığının
iemesi

Kimya
Zayıf Etkileşimler12.
1.
Madde
2.
Madde
Erime -
Kaynama
Noktası
Sebebi
Y
X
X> Y
1.
Hidrojen bağı
II.
Y
Y>Z
Z
Dipol - Dipol
etkileşimi
N
T
T>Z
London kuvvetleri
Yukarıdaki tabloda X, Y, Z ve T moleküllerinin eri-
me-kaynama noktaları kıyaslanmıştır. Tablonun en
sağ sütununda ise erime noktası büyük olan mad-
denin, erime noktasının hangi kuvvet sebebiyle bü-
yük olduğu yazılmıştır.
Buna göre, bu maddeler hakkında verilen aşağı-
daki ifadelerden hangisi yanlıştır?
A) X ve Y molekülleri polar iken Z ve T molekülleri
apolardir.
B) Y ve z moleküllerinde etkin çekim kuvveti di-
pol-dipol etkileşimidir.
C) X molekülü ile su arasında hidrojen bağı oluşur.
D) T molekülünün toplam elektron sayısı Z'den
daha fazladır.
E) T moleküllerinde anlık dipol bulunur.

Kimya
Zayıf Etkileşimler1.
“Benzer benzeri çözer.” Yani polar maddeler polar çö-
zücülerde apolar maddeler apolar çözücülerde daha iyi
çözünürler.
Yukarıda verilen bilgiye göre,
1. CHA
II. NH3
III. CH OH
maddelerinden hangilerinin H,018) içerisinde çözün-
mesi beklenir?
A) Yalnız!
D) I ve II
B) Yalnız II
C) Yalnız III
E) II ve III

Kimya
Zayıf Etkileşimler9.
6. Aşağıdaki moleküllerden hangisinin atomları arasındaki
bağ türü veya molekül polarlığı sınıflandırılması yanlış
verilmiştir? (H, 5B, N, 30, F, 17CI)
Molekül
Atomlar arası bağ türü Molekül polarlığı
5
8
9
A)
Cl2
Apolar kovalent bağ
Apolar
B)
BH3
Polar kovalent bağ
Apolar
C)
NH3
Polar kovalent bağ
Apolar
Polar kovalent bağ
Polar
D) HO
Polar
E)
HF
Polar kovalent bağ

Kimya
Zayıf Etkileşimler87
11.
5.1
4
IP
9. Normal şartlar altında 5,6 litre hacim kaplayan Sog
E
gazı ile ilgili,
I. Kütlesi 20 gramdır.
S
II. 6,02.1023 tane atom icerir.
III.
8 gram CH, gazı ile eşit sayıda molekül içerir.
yargılarından hangileri doğrudur?
(H=1 g/mol, C=12 g/mol, O=16 g/mol, S=32 g/mol,
Avogadro sayısı = 6,02.1023)
A) Yalnız! D) Ivett
C) I ve III
D) Hve th!
E) 1, H ve II
32
Mono
dolo
Tao
7 /
16
2
zau
X
1 22,4
X 516
itle
to
x=0,25
36
