Zayıf Etkileşimler Soruları

Kimya
Zayıf EtkileşimlerC
(B)
London
London
kuvvetleri (dağılım kuvvetle
küller veya atomlardaki elektron dağılımındaki
dalgalanmanın sonucunda oluşur. Örneğin He
atomunda 2 elektron çekirdek etrafında simet-
rik olarak düzenlenmemiş olabilir.
çekirdek
elektron
(Simetrik elektron
dağılımına sahip He)
5:
Simetrik olarak düzenlenmemiş He'de elekt-
ronlar atomun sol tarafında yoğunlaştığından
atomun sol tarafi o anda hafifçe negatif yüke (8)
sahip olurken sağ tarafı hafifçe pozitif yüke (8¹)
sahip olur. Bu anlık yük durumuna "geçici dipol-
luk" ya da "anlık çift dipol" denir.
(Simetrik olmayan
elektron dağılımına
sahip He)
Bir Helyum atomundaki anlık dipol, komşu
atomlardaki anlık dipolü teşvik eder ve bu atom-
lar birbirini çeker.
London kuvvetinin büyüklüğü atom ve mole-
küllerdeki elektron bulutunun büyüklüğü ve mol
kütlesinin artışı ile artar. Bu durum kaynama
noktasının artışına neden olur.
Yukarıdaki paragrafı okuyan bir öğrenci He ve
20 Ne ile ilgili;
Aynı koşullarda 20 Ne'nun kaynama noktası
He'den yüksektir.
U20 Ne, He'ye göre daha kolay polarize olur
He'ün elektron bulutunun hacmi, 20Ne'ninkin-
den fazladır
sonuçlarından hangileri çıkarabilir?
A) Yalnız I
B) Yalnız II
D) I ve III
NİTELİK Yayıncılık
E) I, II ve III
ve Il

Kimya
Zayıf Etkileşimlern
5. Eşit-sayıda moleküDiçeren
m N.K'da 67,2 litre hacim kaplamaktadır.
latm
ac Bu karışımın kütlesi nedir?
(N=14, O=16)
A) 28
B) 32
P.U=n.R.7
1.67,2 = n. 22,4773
6.
Smal
Band
N₂ ve O₂ gazları karışı-
84 96
96 - 180
C) 60 D) 45 E) 90
67,2 = 22,4n → n = 3
Aynı sıcaklık
Kimya
Zayıf Etkileşimler10.
D) II ve III
A) Yalnız I
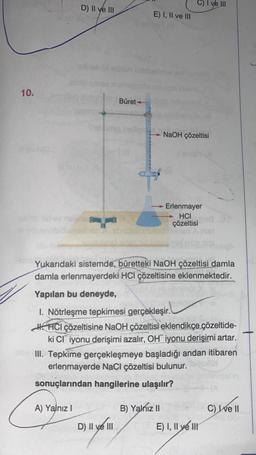
Büret
D) II ve III
E) I, II ve III
6
→NaOH çözeltisi
Yukarıdaki sistemde, büretteki NaOH çözeltisi damla
damla erlenmayerdeki HCI çözeltisine eklenmektedir.
Yapılan bu deneyde,
1. Nötrleşme tepkimesi gerçekleşir.
HHCI çözeltisine NaOH çözeltisi eklendikçe çözeltide-
ki Cl iyonu derişimi azalır, OH iyonu derişimi artar.
III. Tepkime gerçekleşmeye başladığı andan itibaren
erlenmayerde NaCl çözeltisi bulunur.
sonuçlarından hangilerine ulaşılır?
B) Yalnız II
- Erlenmayer
HCI
çözeltisi
I ve III
E) I, II ve II
C) Ive II

Kimya
Zayıf Etkileşimler2. 0 °C ve 1 atm basınçta 11,2 litre hacim kaplayan H₂
gazı için,
I.
1 gramdır.
II. 0,5 moldür.
III. Avogadro sayısı kadar atom içerir.
yargılarından hangileri doğrudur?
(H = 1 g/mol)
A) Yalnız I
D) I ve III
B) Yalnız II
C) I ve II
E) I, II ve III

Kimya
Zayıf EtkileşimlerSoru 2
Aşağıda verilen değişimlerden hangisi
güçlü bağların kırılması sonucu meydana
gelmemiştir?
A) H₂O(s)
B) CaCO3
C) NaCl(K)
D) MgO(K)
E) KCIO3
-
-
H₂ + O₂
CaO+CO,
+ Cl(aq)
Na(aq) +
(g)
Mg2+ + O2
KCI + 0₂

Kimya
Zayıf EtkileşimlerKimyasal Türler Arası Etkileşimler
B
4.1. Şekerin (CH₁20) suda (H₂O) çok iyi çözünmesin-
de rol alan etkileşim türü nedir?
6 12
344D5242
H. Su (H₂O) molekülünde hidrojen (H) ve oksijen (O)
atomları arasındaki etkileşim hangisidir?
III. DNA molekülünün ikili sarmalını bir arada tutan et-
kileşim hangisidir?
IV. Metan (CH₂) bileşiğinin karbontetraklorür (CCI) bile-
şiğinden daha uçucu olması hangi etkileşim ile açık-
lanır?
V. Suyun (H₂O) bitkilerin köklerinden itibaren en uçtaki
yapraklarına kadar iletilmesinde rol alan etkileşim
türü nedir?
Yukarıdaki sorulardan kaç tanesi "hidrojen bağı" ola-
rak yanıtlanamaz?
A) 1
B) 2
(C) 3
D) 4
E) 5

Kimya
Zayıf Etkileşimler8.
Aşağıdakilerden hangisi kimyasal değişime ör-
nek verilebilir?
A) C₂H₂OH'nin (etil alkol) suda çözünmesi
B) Gümüş telin elektrik akımını iletmesi
C) Gaz hâlindeki Ne gazından 1 elektron koparıl-
ması
D) Petrolün damıtılması
E) Demir ve nikel metallerinin eritilerek çelik elde
edilmesi

Kimya
Zayıf Etkileşimler3. Al(OH)3ün sulu çözeltisi ile H₂CO3 sulu çözeltisinin karış-
tırılmasıyla asit - baz tepkimesi gerçekleşir ve sonucun-
da tuz ve su oluşur.
Buna göre, bu tepkimeyi ifade eden net iyon denkle-
mi aşağıdakilerden hangisidir?
A 2Al(OH)3(suda) + 3H₂CO3(suda) →Al₂(CO3)3(suda) + 6H₂O(s)
B) Al(OH)3(suda) + H₂CO3(suda) →AICO.
3(suda) + H₂O(s)
H+
+ OH
(suda) (suda) → H₂O)
(s)
DAI
E) 2A13+
+ CO²-
(suda)
A/³+
(suda)
3 (suda) →AICO 3(suda)
2-
+ 3C03² (suda) → Al2(CO3)3(suda)
II. 2NH₂
III. H2(g)
IV. H₂O
Yukarıda
Bu tepk
teki gib
AJ
An
99 Od
I
1,
11

Kimya
Zayıf EtkileşimlerSAL TEPKİME TÜRLERİ VE HESAPLAMALAR
anlış-
ÖRNEK 13
CS₂ bileşiği yandığında;
1. N₂O3
11. CO₂
Aydın Yayınları
III. SO₂
IV. H₂O
bileşiklerinden hangilerinin oluşması beklenmez?
A) I ve III
ÖRNEK 14
MODÜL 3
CS₂ + O₂ + CO₂ + H₂G+151
B) Il ve IV
D) III ve IV
C) I ve IV
E) II ve III
TYT
lerle ilgili
my

Kimya
Zayıf EtkileşimlerNaCl
(k)
H
2(g)
yukarıda bulunan madde örnekleri için;
I. Fiziksel yöntemler ile ayrılmama
II. Saf madde olma
III. Aynı cins molekül içerme
IV. Hal değiştirirken sıcaklığın değişmesi
yargılarından hangileri ortaktır?

Kimya
Zayıf Etkileşimler4
1. CH4(g) +202(g) → CO2(g)
2. C(k) + O2(g) → CO2(g)
tepkimeleri ile ilgili;
Yalnız III
KİMYASAL TE
D) II ve III
+ 2H₂O(g)
1. İkisi de yanma tepkimesidir.
II. 2. tepkime sentez tepkimesidir.
III. İki tepkimede de toplam enerji azalır.
ifadelerinden hangileri yanlıştır?
p
B) I ve II
E) I, II ve III
C) I ve III

Kimya
Zayıf Etkileşimlerar-
min
na-
t-
I
32. Aşağıdaki tanımlardan hangisi yanlış
verilmiştir?
A) İyonlaşma enerjisi: Gaz hâldeki nötr
atomdan elektron koparmak için gereken
enerjidir.
B) Elektron ilgisi: Gaz hâldeki nötr atomun
elektron alması sırasındaki enerji değişi-
midir.
C) Elektron bulutu: Elektronların bulunma ih-
timalinin yüksek olduğu hacimsel bölgedir.
D) Uyarılmış hâl: Atoma enerji verilerek
elektronun daha yüksek enerji seviyesine
geçme hâlidir.
E) Temel hâl: Bağ elektronlarını çekme hâlidir.

Kimya
Zayıf EtkileşimlerAtom ve Periyodik Sistem.
15. Metaller bileşik oluştururken;
I. Kimyasal özellikleri değişir.
II. Elektron sayıları artar.
III. Proton ve nötron sayıları değişmez.
bilgilerinden hangisi ya da hangileri doğrudur?
A) Yalnız I
B) Yalnız II C) Yalnız III
E) I, II ve III
D) I ve III
19. Periyodik
mentlerle
hangisi d
H
Na
Ca

Kimya
Zayıf Etkileşimler10.
H
B
H
BH3
H
Yukarıda BH3 molekülünün Lewis elektron nokta yapısı
verilmiştir.
Buna göre, aşağıdaki ifadelerden hangisi yanlıştır?
B atomu oktetini tamamlamamıştır.
BH 1A grubu elementidir.
C) Bileşiğin suda çözünmesi beklenir.
D) Molekül içindeki bağlar polar kovalenttir.
E) B atomunun değerlik elektronlarının hepsi bağ yapımı-
na katılmıştır.

Kimya
Zayıf EtkileşimlerKİMYA
9
Kimyasal türler arasındaki etkileşim sırasındaki enerji değişi-
mi genellikle 40 kJ/mol'den küçük ise zayıf etkileşim, 40 kJ/
mol'den büyük ise güçlü etkileşim oluşur.
1.
Ag(s) → Ag(k)
II.
O₂(g) + H₂O(s) → O₂(suda)
III. H₂(g) + O₂(g) → H₂O(g)
IV. Na(k) +
Cl₂(g)
Cl₂(g) → NaCl(k)
V. 2H(g)
H₂(g)
Buna göre, yukarıda verilenlerden hangisinde enerji
değişimi 40 kJ/mol'den küçüktür?
A) I
B) Il
C) III
→
D) IV E) V

Kimya
Zayıf Etkileşimlermyrama
CH₂OH
HCI
C:
H₂O
a
BF 3
Yukarıdaki maddelerin;
F-O-N
H₂O GI!!
a: Kendi molekülleri arasında hidrojen bağı oluşturanlar
b:
A) H₂O, H₂S
CH₂OH
B)
CH₂OH, H₂O
C) CH₂OH, H₂O
D) CH₂OH, HCH
E) H₂O, HCI
Etkin etkileşim türü dipol-dipol etkileşimi olanlar
Sadece London kuvvetleri ile bir arada tutulanlar
apple ap
şeklinde sınıflandırılması aşağıdakilerden hangisinde
doğru verilmiştir? S
21816)
b
H₂S
HCI, BF3
He
BF H₂S
HCI, H₂S
H₂S, H₂O
CH₂OH, H₂S
He
C
HCI, He
BF, He
3'
BF3, He
He, BF3
