Reaksiyon Hızı Soruları
Kimya
Reaksiyon HızıMolekül yüzdesi
1
X
Y
Kinetik
Enerji
Molekül yüzdesi
||
Y
X
Hız
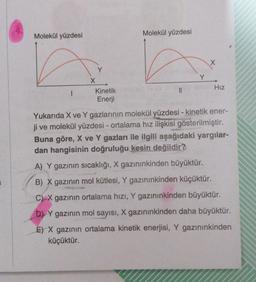
Yukarıda X ve Y gazlarının molekül yüzdesi - kinetik ener-
ji ve molekül yüzdesi - ortalama hız ilişkisi gösterilmiştir.
Buna göre, X ve Y gazları ile ilgili aşağıdaki yargılar-
dan hangisinin doğruluğu kesin değildir?
A) Y gazının sıcaklığı, X gazınınkinden büyüktür.
B) X gazının mol kütlesi, Y gazınınkinden küçüktür.
C) X gazının ortalama hızı, Y gazınınkinden büyüktür.
D) Y gazının mol sayısı, X gazınınkinden daha büyüktür.
E) X gazının ortalama kinetik enerjisi, Y gazınınkinden
küçüktür.
![a
Qor
Üç adımda gaz fazında gerçekleşen
2A + B → F
AH = -80 kJ
tepkimesinin mekanizması,
2. Adım: A + C → K+L
3. Adım: D + K+L→ F
(hızlı)
(çok hızlı)
olduğuna göre, tepkime hız denklemi aşağıdaki-
lerden hangisidir?
A) r = k· [A]².[B]
C) r = k· [A] [K]
B) r = k· [A] [B]
D) r = k. [K]²
E) r = k [A]² [B] [F]](https://media.kunduz.com/media/question/seo/raw/20220721150235095826-4370496.jpg?w=256)
Kimya
Reaksiyon Hızıa
Qor
Üç adımda gaz fazında gerçekleşen
2A + B → F
AH = -80 kJ
tepkimesinin mekanizması,
2. Adım: A + C → K+L
3. Adım: D + K+L→ F
(hızlı)
(çok hızlı)
olduğuna göre, tepkime hız denklemi aşağıdaki-
lerden hangisidir?
A) r = k· [A]².[B]
C) r = k· [A] [K]
B) r = k· [A] [B]
D) r = k. [K]²
E) r = k [A]² [B] [F]

Kimya
Reaksiyon Hızı10. Sabit hacimli kaba PCl3 ve Cl₂ gazları konularak sabit sıcak
likta,
PCI3(g) + Cl₂(g) → PCl5(g)
tepkimesi gerçekleştiriliyor.
Tepkime süresince,
Birim zamanda gerçekleşen etkin çarpışma sayısı
Tepkime hızı
fil. Oluşan PCI5 gazı miktarı
niceliklerinden hangileri artar?
A) Yalnız I
B) Yalnız II
1.
D) II ve III
AX
31.
AM
3
C) Yalnız III
E) I, II ve III
UNYASAL D
Eiriksel ve

Kimya
Reaksiyon Hızı6.
Sabit hacimli kapalı bir kapta, sabit sıcaklıkta gerçek-
leşen,
tepkimesi
yanlıştır?
2X(g) + ISI2Y(g) + Z(g)
ile ilgili aşağıdaki açıklamalardan hangisi
A) X gazının ayrışma hızı zamanla azalır.
B) Z gazının oluşma hızı zamanla artar.
C) Gaz özkütlesi zamanla değişmez.
D) Gaz basıncı zamanla artar. X
E) Y gazının kısmi basıncı zamanla artar.

Kimya
Reaksiyon Hızı11.
Xile Y₂ gazları arasında oluşan ve tek cins ürünün oluştuğu
tepkime ile ilgili şu bilgiler veriliyor;
- X gazının harcanma hızı, Y2 gazının harcanma hızının 3/2
-
katıdır.
- Ürünün oluşma hızı, Y₂ gazının harcanma hızının yarısı-
-
dır.
Buna göre, ürünün formülü aşağıdakilerin hangisinde
doğru verilmiştir?
A) X3Y4
D) XY 3
B) X₂Y3
E) X3Y2
C) XY ₂
![Jiz
18. Gaz fazında gerçekleşen
X₂ + 3Y2
-
2XY3
tepkimesi için belirli bir sıcaklıktaki deney sonuçları aşa-
ğıda verilmiştir.
Tepkime hızı
Deney
[X₂]
[Y₂]
mol
No (mol/L)
(mol/L)
L.s
1
0,1A
0,1
1.10-5-
2
0,1
0,2
2.10-5
3
0,2
0,4
16.10-5
Buna göre, bu tepkime ile ilgili,
1. En az iki basamaklıdır.
II. Hız bağıntısı; k. [X₂] [Y₂]³ şeklindedir.
2
-1
S dir.
III. Hız sabitinin birimi, mo
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız III
D) II ve III
C) I ve II
E) I ve III](https://media.kunduz.com/media/question/seo/raw/20220614191030620876-4514047.jpg?w=256)
Kimya
Reaksiyon HızıJiz
18. Gaz fazında gerçekleşen
X₂ + 3Y2
-
2XY3
tepkimesi için belirli bir sıcaklıktaki deney sonuçları aşa-
ğıda verilmiştir.
Tepkime hızı
Deney
[X₂]
[Y₂]
mol
No (mol/L)
(mol/L)
L.s
1
0,1A
0,1
1.10-5-
2
0,1
0,2
2.10-5
3
0,2
0,4
16.10-5
Buna göre, bu tepkime ile ilgili,
1. En az iki basamaklıdır.
II. Hız bağıntısı; k. [X₂] [Y₂]³ şeklindedir.
2
-1
S dir.
III. Hız sabitinin birimi, mo
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız III
D) II ve III
C) I ve II
E) I ve III
![2. BrO3(aq) + 5Br (aq) + 6H*(aq)
3Br₂(aq) + 3H₂O(s)
Bromat iyonunun bromür ile indirgenme tepkimesi yukarıda
verilmiştir. Yapılan bir sıra deney sonucunda hız ifadesi,
r = k. [BrO3].[Br].[H]2
şeklinde bulunmuştur.
Buna göre;
1. Mekanizmalı bir tepkimedir.
II. Tepkime Br ye göre 1. derecedendir.
III. Çözeltiye bir miktar baz eklenirse tepkime hızı artar.
yargılarından hangileri doğrudur?
A) Yalnız I
B) I ve II
C) I ve III
D) II ve III
E) I, II ve III](https://media.kunduz.com/media/question/seo/raw/20220614183303077186-3539241.jpg?w=256)
Kimya
Reaksiyon Hızı2. BrO3(aq) + 5Br (aq) + 6H*(aq)
3Br₂(aq) + 3H₂O(s)
Bromat iyonunun bromür ile indirgenme tepkimesi yukarıda
verilmiştir. Yapılan bir sıra deney sonucunda hız ifadesi,
r = k. [BrO3].[Br].[H]2
şeklinde bulunmuştur.
Buna göre;
1. Mekanizmalı bir tepkimedir.
II. Tepkime Br ye göre 1. derecedendir.
III. Çözeltiye bir miktar baz eklenirse tepkime hızı artar.
yargılarından hangileri doğrudur?
A) Yalnız I
B) I ve II
C) I ve III
D) II ve III
E) I, II ve III

Kimya
Reaksiyon HızıOrbital Yayınları
3. Bir tepkimenin hız sabiti k;
1. Sıcaklık
II. Katalizör
III. Reaktiflerin derişimi
niceliklerinden hangileri ile değişir?
A) Yalnız I
B) Yalnız II
D) I ve II
E) I ve III
C) Yalnız III

Kimya
Reaksiyon Hızı20. 2N2O(g) 2N2(g) + O2(g)
1
tepkimesi başladıktan 150 s sonra ortamda
0,0030 mol/L 02 oluşmaktadır.
Buna göre, N₂O'nun ortalama tükenme hızı kaç
mol L-1 s-1 dir?
A) 4,0 x 10-4
B) 2,0 x 10-4
C) 4,0 x 10-5
24
C
D) 2,0 x 10-5
E) 4,0 x 10-6
![fast AYT8 no
18. Kapalı bir kapta gerçekleşen,
4HBr(g) + O2(g) → 2H₂O(g) + 2Br2(g)
tepkimesinin hız ifadesi r = k. [HBr][0₂] şeklindedir.
Buna göre;
emd
162
1. Tepkime mekanizmalıdır.
II. Kap hacmi yarıya düşürülürse tepkime hızı iki ka-
tına çıkar. Ulaum X sixtbisote tidee sds>
lebrióp isso 0
III. Tepkime ikinci derecedendir.
yargılarından hangileri doğrudur?
llop shiee
notei
A) Yalnız I
B) I ve II
18h8
D) I ve III
E) I, II ve III
ob holigned nisbnnsligisy
(31-01-H $1 = 0)
C) II ve III](https://media.kunduz.com/media/question/seo/raw/20220614124808800517-1473048.jpeg?w=256)
Kimya
Reaksiyon Hızıfast AYT8 no
18. Kapalı bir kapta gerçekleşen,
4HBr(g) + O2(g) → 2H₂O(g) + 2Br2(g)
tepkimesinin hız ifadesi r = k. [HBr][0₂] şeklindedir.
Buna göre;
emd
162
1. Tepkime mekanizmalıdır.
II. Kap hacmi yarıya düşürülürse tepkime hızı iki ka-
tına çıkar. Ulaum X sixtbisote tidee sds>
lebrióp isso 0
III. Tepkime ikinci derecedendir.
yargılarından hangileri doğrudur?
llop shiee
notei
A) Yalnız I
B) I ve II
18h8
D) I ve III
E) I, II ve III
ob holigned nisbnnsligisy
(31-01-H $1 = 0)
C) II ve III
![DENEME SINAVI 23
13. Iki basamakta gerçekleştiği bilinen,
3
2
2N₂O(g)
0₂(g) NO₂(g)
tepkimesinin hızlı basamağı,
N₂O(g) + O₂(g)
>2NO(g)
2
şeklindedir.
Buna göre, bu tepkimenin hız denklemi
aşağıdakilerin hangisinde doğru verilmiştir?
A) Hız = K. [NO₂]²
B) Hız = k. [N₂0] [0₂]³/²
C) Hız = k.[NO]² [0₂]
D) Hız =
=k-[N₂0] [0₂]¹/2
E) Hız = k. [NO]²
-](https://media.kunduz.com/media/question/seo/raw/20220614100634721910-3735678.jpg?w=256)
Kimya
Reaksiyon HızıDENEME SINAVI 23
13. Iki basamakta gerçekleştiği bilinen,
3
2
2N₂O(g)
0₂(g) NO₂(g)
tepkimesinin hızlı basamağı,
N₂O(g) + O₂(g)
>2NO(g)
2
şeklindedir.
Buna göre, bu tepkimenin hız denklemi
aşağıdakilerin hangisinde doğru verilmiştir?
A) Hız = K. [NO₂]²
B) Hız = k. [N₂0] [0₂]³/²
C) Hız = k.[NO]² [0₂]
D) Hız =
=k-[N₂0] [0₂]¹/2
E) Hız = k. [NO]²
-
![00:52
Q%18
B
B
2X+Y+Z-K+2Z
tepkimesi gaz fazında gerçekleşmekte ve aynı sıcaklıkta
derişimlere bağlı deney sonuçları tabloda verilmiştir.
Hız
Deney [X]
[Y]
[Z]
(mol/L.s)
1
0,01
0,2
0,01
1.10-3
2
0,01
0,2
0,03
1.10-3
3
0,02
0,2
0,02
4.10-3
4
0,02
0,4
0,03
8.10-3
Buna göre, aşağıdakilerden hangisi yanlıştır?
A) r= k[X]2 [Y]'dir.
B) Tepkime derecesi 3'tür.
CC) Tepkime mekanizmalıdır.
D) Iz sabiti k'nin değeri 0,5'tir
E) Yavaş basamak 2X + Y
1
|||
AYT DENEME SINAVI
25.
: 0
Ürün şeklinde olabilir.
27.
28.](https://media.kunduz.com/media/question/seo/raw/20220613215252321971-4554763.jpg?w=256)
Kimya
Reaksiyon Hızı00:52
Q%18
B
B
2X+Y+Z-K+2Z
tepkimesi gaz fazında gerçekleşmekte ve aynı sıcaklıkta
derişimlere bağlı deney sonuçları tabloda verilmiştir.
Hız
Deney [X]
[Y]
[Z]
(mol/L.s)
1
0,01
0,2
0,01
1.10-3
2
0,01
0,2
0,03
1.10-3
3
0,02
0,2
0,02
4.10-3
4
0,02
0,4
0,03
8.10-3
Buna göre, aşağıdakilerden hangisi yanlıştır?
A) r= k[X]2 [Y]'dir.
B) Tepkime derecesi 3'tür.
CC) Tepkime mekanizmalıdır.
D) Iz sabiti k'nin değeri 0,5'tir
E) Yavaş basamak 2X + Y
1
|||
AYT DENEME SINAVI
25.
: 0
Ürün şeklinde olabilir.
27.
28.

Kimya
Reaksiyon Hızıb
Orbital Yayınları
Com 1.
10. Sabit hacimli bir kapta tek basamakta gerçekleşen,
A(g) + B(g) →→→ C(g)
Tepkimesinin hız sabiti k = 1.10-6 L.mol-1.s-1 dir.
0,4'er mol A ve B alınarak gerçekleştirilen tepkimenin
hızı 4.10-8 M/s olduğuna göre, tepkime kabının hacmi
kaç litredir?
A) 0,1
B) 0,2
C) 1
D) 2
E) 4
00(0
Morn
L
8(2
![21.
22.
A
H₂(g)
+21Cl(g) → 12(g) + 2HCl (g)
tepkimesi sabit sıcaklıkta iki basamakta gerçekleşmektedir.
Tepkimenin hızlı basamağı
HI(g) + ICI (g)
12(g) + HCl (g)
şeklinde olduğuna göre, tepkimenin hız denklemi aşa-
ğıdakilerden hangisinde doğru olarak verilmiştir?
A) Hız = K[H₂][ICI]²
k
B) Hız = K[H₂]
C) Hız = K[H₂] [ICI]
E) Hiz=K[ICI]²
Hız
H₂ + $141 HCl + HI
⇒ N₂O4(g)
2NO(g)
O2(g)
+
Hiz=K[H₂][IC]
oklıkta kabın hacmi](https://media.kunduz.com/media/question/seo/raw/20220613164719681119-1514981.jpeg?w=256)
Kimya
Reaksiyon Hızı21.
22.
A
H₂(g)
+21Cl(g) → 12(g) + 2HCl (g)
tepkimesi sabit sıcaklıkta iki basamakta gerçekleşmektedir.
Tepkimenin hızlı basamağı
HI(g) + ICI (g)
12(g) + HCl (g)
şeklinde olduğuna göre, tepkimenin hız denklemi aşa-
ğıdakilerden hangisinde doğru olarak verilmiştir?
A) Hız = K[H₂][ICI]²
k
B) Hız = K[H₂]
C) Hız = K[H₂] [ICI]
E) Hiz=K[ICI]²
Hız
H₂ + $141 HCl + HI
⇒ N₂O4(g)
2NO(g)
O2(g)
+
Hiz=K[H₂][IC]
oklıkta kabın hacmi
![D) I ve III
m = ņ
1=4145
21. Tepkime hız bağıntısı k. [X]. [Y]2 şeklinde olan tepkime ile
ilgili olarak;
Sıcaklık (°C)
[X] mol/L
[Y] mol/L
50
1.
0,2
0,1
2.
0,2
0,1
25
3.
0,1
0,2
50
bilgileri veriliyor.
Buna göre, tepkime hızları (r) ve hız sabitleri (k)
arasındaki ilişki aşağıdakilerden hangisinde doğru
verilmiştir?
Hız (r)
Hız sabiti (k)
AX
r₁ > 13 > 2
K₂ > K₁=k3
BY
r2 >3 > r₁
K3 > K₁ > K₂
C)
13 >₁ > 12
K₁=k3 > K₂
1
D
1₁ > T₂ > 13
K₁=k3 > K₂2
E
r3 > r₁ > 12
K3 > K₁ > K₂
36
n=015
14](https://media.kunduz.com/media/question/seo/raw/20220612190811866180-1759509.jpeg?w=256)
Kimya
Reaksiyon HızıD) I ve III
m = ņ
1=4145
21. Tepkime hız bağıntısı k. [X]. [Y]2 şeklinde olan tepkime ile
ilgili olarak;
Sıcaklık (°C)
[X] mol/L
[Y] mol/L
50
1.
0,2
0,1
2.
0,2
0,1
25
3.
0,1
0,2
50
bilgileri veriliyor.
Buna göre, tepkime hızları (r) ve hız sabitleri (k)
arasındaki ilişki aşağıdakilerden hangisinde doğru
verilmiştir?
Hız (r)
Hız sabiti (k)
AX
r₁ > 13 > 2
K₂ > K₁=k3
BY
r2 >3 > r₁
K3 > K₁ > K₂
C)
13 >₁ > 12
K₁=k3 > K₂
1
D
1₁ > T₂ > 13
K₁=k3 > K₂2
E
r3 > r₁ > 12
K3 > K₁ > K₂
36
n=015
14

Kimya
Reaksiyon Hızıve-
my favorite c
Fine
Jumba
AYT/Fen Bilimleri
27. Aşağıda bir tepkimeye ait molekül sayısı-kinetik enerji
grafiği verilmiştir.
Molekül sayısı
T₁
→ Kinetik enerji
E₂
E₁
Buna
göre tepkime için;
I. T₂ sıcaklığındaki ortalama kinetik enerjisi, T₁ sıcak-
lığındakinden büyüktür,
II. Sıcaklığı T, den T₂ ye getirildiğinde aktifleşme ener-
jisi artar,
III. Sıcaklığı T, ve aktifleşme enerjisi E, iken hızı en
fazladır
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız III
C) I ve II
D) II ve III
cho
T₂
E) I, II ve III
